Autofagia e Autolisosomi nei gliosarcomi
Osservazioni ultrastrutturali
Prof. Luigi Cuccurullo
Emerito di Anatomia Patologica
Il gliosarcoma è una variante del glioblastoma; esso è caratterizzato da tessuti aventi una morfologia bifasica, disposti in aree separate o commiste, uno con aspetto gliale, l’altro con aspetto fenotipico mesenchimale (WHO, 2016).
E’ stata dimostrata la monoclonalità delle sopracitate due popolazioni cellulari ed è stato sostenuto essere la componente mesenchimale una espressione metaplasica delle cellule gliali (WHO, 2016).
Inoltre, le aberrazioni genetiche, il profilo clinico e le prospettive prognostiche ripetono quelle del glioblastoma (J. Of Neuro-oncology 2005; 74: 59-63).
I reperti qui di seguito commentati si riferiscono a casi di gliosarcoma aventi come componente fenotipica mesenchmale una morfologia riferibile a fibrosarcoma scarsamente differenziato.
L’attenzione è stata rivolta in modo uguale alle due componenti dei casi osservati nel valutare e descrivere i processi regressivi dei mitocondri. dell’ergastoplasma rugoso e liscio,dei focolai di autofagia e di auto lisosomi, dei gravi processi di vacuolizzazione fino alla citolisi.
Le alterazioni regressive mostrano la stessa tipologia nelle due componenti del gliosarcoma e rivelano una realtà composita ed interdipendente,poiché nelle stesse cellule coesistono in grado diverso alterazioni di tutte le sub- strutture dianzi citate.
Ciò è conseguente alla esistenza di meccanismi di mutua induzione secondo i quali l’avvio di un processo disfunzionale a carico dei mitocondri o del reticolo endoplasmico progressivamente(se non si recupera l’omeostasi) coinvolge tutti gli altri organelli fino a concludersi con il quadro di una delle morti cellulari.
Questa realtà composita, quale carattere generale di bio-morfologia cellulare,non può essere descritta nel suo insieme,ma richiede una esposizione selettiva per singoli organelli,riservando alla fine una operazione di sintesi per esprimere un giudizio valutativo su le alterazioni reperite.
La linea espositiva qui scelta si articola secondo diversi paragrafi: il primo descrive i caratteri generali ultrastrutturali di questo tumore, gli altri ,a seguire, riportano le alterazioni dei mitocondri,dell’ergastoplasma,del reticolo endoplasmico,dei lisosomi con i focolai di autofagia e di auto lisosomi.
CARATTERI GENERALI
La popolazione cellulare è iperdensa,mostra un indice di coesione molto variabile con rare strutture giunzionali;la morfologia ultrastrutturale degli elementi è pleomorfa, condizione aggravata dai subentranti e progressivi processi regressivi e destrutturanti.
Sono presenti elementi fusati,ovoidali,poligonali di diverse volumetrie;come dato costante,si riscontra un nucleo voluminoso,irregolare,con cromatina addensata alla periferia e una quota citoplasmatica abitualmente esigua. La composizione del citoplasma di queste cellule appare variabile sia per squilibri quantitativi dei vari organelli, sia per i subentranti processi regressivi.
MITOCONDRI
In tutte le cellule, in condizioni di normalità o di patologie,e tra queste anche nelle cellule neoplastiche si riscontrano alterazioni mitocondriali semplici o complesse che fanno parte dell’ampio capitolo delle disfunzioni mitocondriali.
In queste cellule è frequente il riscontro di due tipologie mitocondriali: una rappresentata da mitocondri rigonfi, vacuolizzati e deprivati delle creste; l’altra è data da mitocondri piccoli, coartati, con matrice densa e creste mascherate da tale materiale.
Queste modificazioni sono spesso correlate a uno stato di ipossia cronica; si ritiene che i mitocondri rigonfi siano particolarmente sensibili a uno stato di sofferenza ipossica, mentre quelli aventi una matrice addensata sono “ tolleranti” a tale situazione cronica (J. Electron Microsc. 2008; 57: 33-39).
E’ stato accertato che nelle cellule neoplastiche si ha una attività energetica sregolata, associata a disfunzione mitocondriale, a mutazione del mit/DNA, ad un aumento del livello di ossigeno reattivo (ROS);a tutto ciò si deve aggiungere un aumento del Ca2+, degli onco-metaboliti,con alterazioni dei soppressori tumorali,e come fattore non meno importante si rileva la soppressione della proteina p53, proteina che regola la respirazione mitocondriale e il metabolismo cellulare. (Cell Cycle 2013; 12: 172-82) (Exp. Biol. Med. 2016; 241: 1281-95).
Nelle cellule dei gliosarcomi qui esaminati si reperta una quota esigua di mitocondri;essi mostrano una doppia morfologia: La maggior parte è costituita da mitocondri piccoli,rotondeggianti,compatti,coartati e contenenti un ridotto numero di creste.
In rare cellule,invece,si repertano mitocondri rigonfi,lucenti,trasparenti e deprivati in modo parziale o totale delle creste. Frequentemente,i mitocondri così rigonfi presentano alterazioni di permeabilità o rottura della membrana mitocondriale esterna con rilascio del contenuto nel citosol.
ERGASTOPLASMA
In diverse condizioni di patologia (malattie neurodegenerative, diabete, disordini metabolici, stress ossidativi, infezioni, flogosi,etc.) e tra queste anche nelle neoplasie maligne si può riscontrare l’ergastoplasma in condizioni di stress. (Genes Cancer 2010; 1:764-778) (Cell Biol. 2012; 197: 857-867)
Al microscopio elettronico l’ergastoplasma in stato di stress appare con cisterne dilatate e ricolme di materiale amorfo, debolmente elettropaco.
Questo materiale è costituito da proteine non correttamente ripiegate ed assemblate e pertanto non trasportabili e non utilizzabili e di conseguenza possono subire un processo di degradazione (ERAD= ER- Associated Degradation).
Nelle situazioni di stress temporaneo si ha un ripristino dell’omeostasi dell’ergastoplasma mediante il sistema UPR (Unfolded Protein Response); diversamente, se lo stato di stress dovesse prolungarsi (come si riscontra nelle cellule neoplastiche) si ha una situazione di stress estesa all’intera cellula,con successiva attivazione di un processo di autofagia e infine con l’instaurarsi di un processo di morte cellulare (Am J. Pathol. 2007; 171: 513-24) (FEBS 2016; 283: 498-509).
Anche nelle cellule dei gliosarcomi quì rivisitati, si repertano disfunzioni ergastoplasmatiche; infatti si evidenziano tratti della rete ergastoplasmatiche con cisterne dilatate e ricolme di materiale amorfo, debolmente elettropaco. In un minor numero di cellule questa disfunzione si appalesa sotto forma di fasci iperdensi di sub strutture ergastoplasmatiche variamente orientate,spesso con cisterne ectasiche e occupanti una ampia area del citoplasma.
RETICOLO ENDOPLASMICO
Anche il reticolo endoplasmico mostra segni ultrastrutturali di stress sia in associazione all’ergastoplasma sia in situazioni univoche.
Infatti,si repertano cellule di gliosarcoma con l’ ampio citoplasma occupato quasi interamente da queste formazioni; esse sono molto numerose, si trovano tra loro adese e mostrano le loro cisterne ectasiche o micro cistiche, creando così in una visione panoramica una immagine di aspetto cribroso .Lo spazio interno alle cisterne è apparentemente privo di contenuto, o, più raramente, è occupato da materiale amorfo, debolmente elettropaco.
LISOSOMI
I lisosomi sono attivamente partecipi nei processi di crescita neoplastica e nell’impianto dei focolai metastatici a seconda del loro numero, alla loro distribuzione e alla attività degli enzimi da essi sintetizzati e rilasciati. (Ann. N.Y. Acad. Sci. 2016; 1371:45-54).
Come è già ampiamente documentato, i lisosomi sono determinanti nei processi di apoptosi, di autofagia e di necrosi; a tali eventi è necessario aggiungere anche la esistenza della morte cellulare lisosomiale indotta da enzimi lisosomiali riversati nel citosol. (FEBS J, 2015; 282: 4279-4288).
Tutto ciò viene attivato per la rottura della membrana lisosomiale o più frequentemente per fenomeni di permeabilizzazione della stessa con effetti citotossici su il metabolismo cellulare e su gli organelli citoplasmatici. (Redox Rep. 2001; 6: 91-97) (J. Cell Biol. 2001; 153: 999-1010).
(Biochimica et Biophysica Acts 2009; 1793: 746-54) (Cell Death and Differentiation 2010; 17: 922-930).
Nelle cellule di gliosarcoma qui esaminate si repertano con scarsa frequenza lisosomi primari o secondari;i primi appaiono come corpi densi,compatti, elettropachi,immersi nel citosol ;i secondi si presentano quali strutture cave delimitate da una membrana a monostrato.
AUTOFAGOSOMI E AUTOLISOSOMI
L’autofagosoma è un focolaio vescicoloso endocellulare,di diverse dimensioni,di forma sferoidale,delimitato da una membrana a doppio strato;al suo interno si ritrovano materiali biologici eterogenei di aspetto granuloso,filamentoso,amorfo,tubulare e nei focolai voluminosi anche organelli citoplasmatici o frammenti nucleari.
Dopo questa fase di accumulo del cargo,segue quella della fusione tra l’autofagosoma e un lisosoma con formazione di una nuova struttura indicata con il termine di autolisosoma.
Tutto l’insieme così fuso viene sottoposto a un processo di degradazione da parte delle idrolasi lisosomiali e i prodotti così degradati,ridotti a entità di molecole semplici sono riversati nel citosol per essere riutilizzati nei processi di biosintesi o di attività energetiche. ( Antioxid Redox Signal 2014;20:460-473).
Gli autolisosomi inizialmente mostrano una doppia membrana di contorno,successivamente la membrana interna viene demolita dagli enzimi lisosomiali e appaiono come sub strutture vescicolose delimitate da una membrana a monostrato; pertanto si distinguono con difficoltà dai lisosomi secondari.(Margit Pavelka, Jurgen Roth: Functional Ultrastructure,Springer Verlag, 2015).
Tutto ciò è espressione biologica del processo di autofagia,quale meccanismo dinamico e attivo in numerose situazioni di fisiologia e patologia cellulare Essa si manifesta e si evolve in quanto è indotta da fattori nutrizionali,metabolici,ossidativi,infettivi,degenerativi, genotossici, proteolitici, neoplastici e in quelle situazioni da stress del reticolo endoplasmico e da disfunzione mitocondriale che mettono a rischio l’omeostasi cellulare.(Science,2011;334:358-362:)(Cell,2012;148:1145-115) (Nat.Rev.Cancer,2012;12:401-410).
Nel citoplasma delle cellule di gliosarcoma esaminate sono stati riscontrati con frequenza focolai di autofagosomi e di autolisosomi; i primi si riconoscono quali corpi ovoidali o rotondeggianti i quali sono demarcati da una membrana a doppio contorno e contengono nel loro spazio cavo materiale granuloso,filamentoso ed amorfo; i secondi,gli autolisosomi, sono delimitati da una membrana a monostrato,spesso notevolmente ispessita per sovrapposizione di materiale amorfo;il loro contenuto è rappresentato da materiale biologico in varie fasi di degradazione.
Commento
L’esame dei reperti ultrastrutturali, dianzi descritti ha mostrato la ripetitività di alcune alterazioni, tutte di tipo regressivo con tendenza ad evolvere verso la degradazione e la destrutturazione fino alla fase conclusiva della citolisi.
Le alterazioni riscontrate al microscopio elettronico,sebbene siano diverse per tipologia e gravità,si ripetono con molta frequenza e pertanto devono essere considerate non occasionali,bensì inerenti alle condizioni biomorfologiche e metaboliche e tutto ciò rappresenta un dato significativo che richiede una interpretazione patogenetica.
Frequentemente sono sti riscontrate nell’ambito della stessa cellula la coesistenza di alterazioni diverse e allo stesso modo è abituale il riscontro di elementi cellulari tra loro coesi,dei quali uno si trova in uno stato di necrosi apoptotica,gli altri sono in uno stato di necrosi post-vacuolizzazione lisosomiale.
I dati alterativi presentatisi con maggiore incidenza sono qui di seguito riassunti e commentati:
1. Ridotto numero di mitocondri; quelli presenti sono piccoli, rotondeggianti, coartati, addensati e poveri di creste. Tale reperto è indicativo di uno stato di disfunzione.
2. Presenza di quote dominanti in alcune cellule di ergastoplasma rugoso e in altre di quello liscio. Ambedue le sub strutture si ritrovano in molte cellule in stato di stress.
- 3. Cellule sedi di vacuoli confluenti e di ampie vescicole apparentemente prive di contenuti e cellule sedi di lisi per rottura della membrana plasmatica.
- 4. In tale contesto si ritrovano focolai di autofagia e voluminosi autolisosomi.
In particolare, i reperti riferibili alle attività lisosomiali e alla presenza di focolai di autofagia nei glioblastomi (dei quali i gliosarcomi fanno parte) erano già stati descritti in letteratura, sia su campioni chirurgici non irradiati sia su quelli preventivamente irradiati. (Autophagy, 2008; 4: 467-475) (NeuroOncol. 2010; 12: 328-340) (Cancer Biol. Ther. 2014; 15: 1468-1478).
La patogenesi di questi processi regressivi evolventi verso la necrosi cellulare apoptotica, autofagica e lisosomiale viene ipotizzata nello stato di ipossia cronica nel quale versano le cellule di una neoplasia in uno stato di attiva proliferazione. E’ ben noto che la rete vascolare neoformata è insufficiente per quantità e per modalità di distribuzione a provvedere alle esigenze metaboliche di una massa cellulare in rapida crescita.
Questa condizione di ipossia cronica provoca una riduzione del traffico di proteine, e un aumento di proteine unfolded e misfolded, inducente le condizioni biochimiche di uno stato di stress (Cell Death Dis. 2016; 7; 2434).Nel contempo si ha un incremento di metaboliti e di bioossidanti che contribuiscono ai danni dell’ergastoplasma, del reticolo endoplasmico e dei mitocondri (J. Clin. Inves 2015; 125: 42-46) (Nat. Rev. Mol. Cell. Biol. 2014; 15: 81-94) (Cell Res. 2012; 22: 43-61).
La persistenza di queste condizioni di stress dell’ergastoplasma, del reticolo endoplasmico e di disfunzioni mitocondriale,aggravate da fenomeni di alterata permeabilizzazione e di rottura delle membrane di queste sub strutture favoriscono l’attivazione dei processi di autofagia con formazione di autolisosomi. (Cancer Res. 2012; 72: 1773-83).
Fig.1 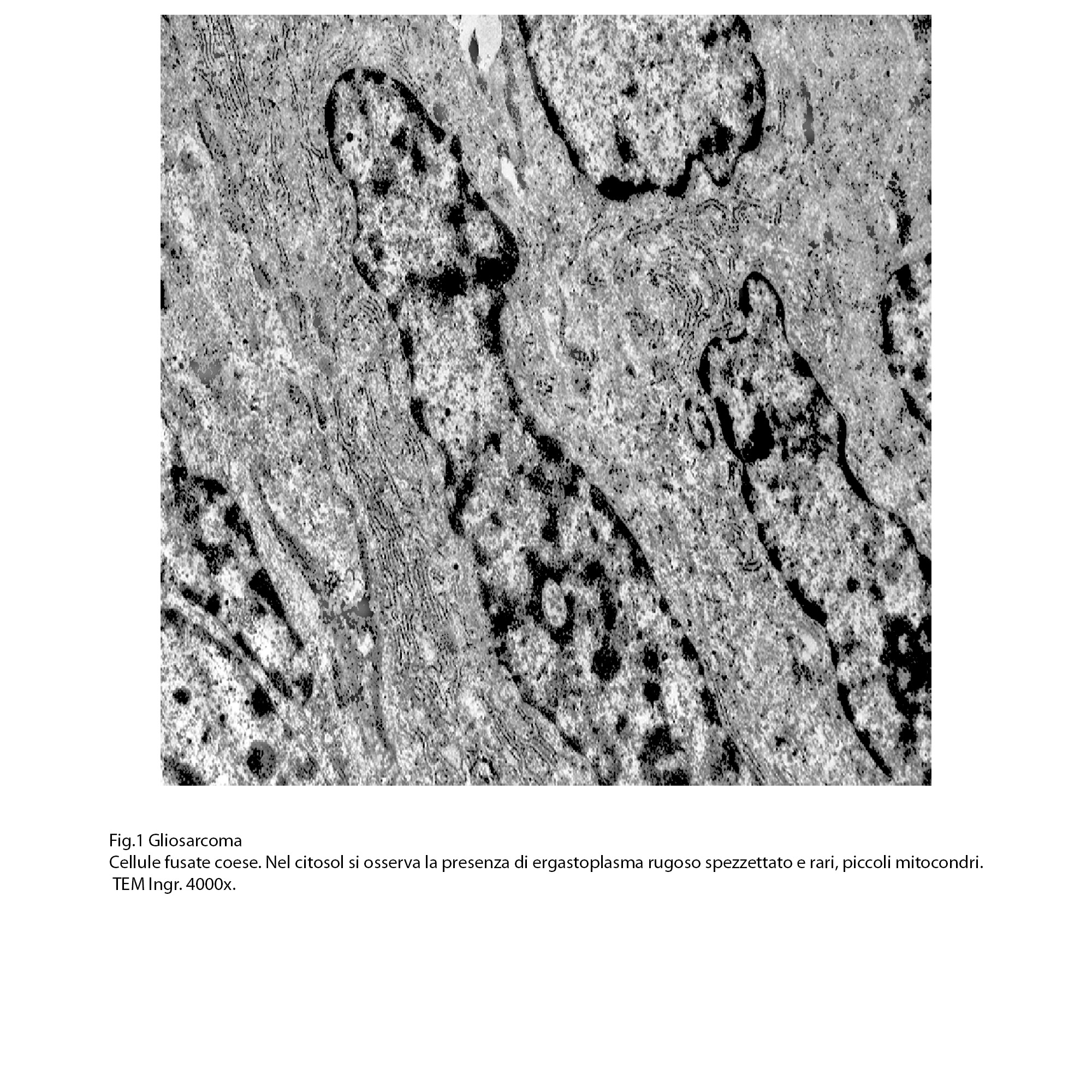 Fig.2
Fig.2 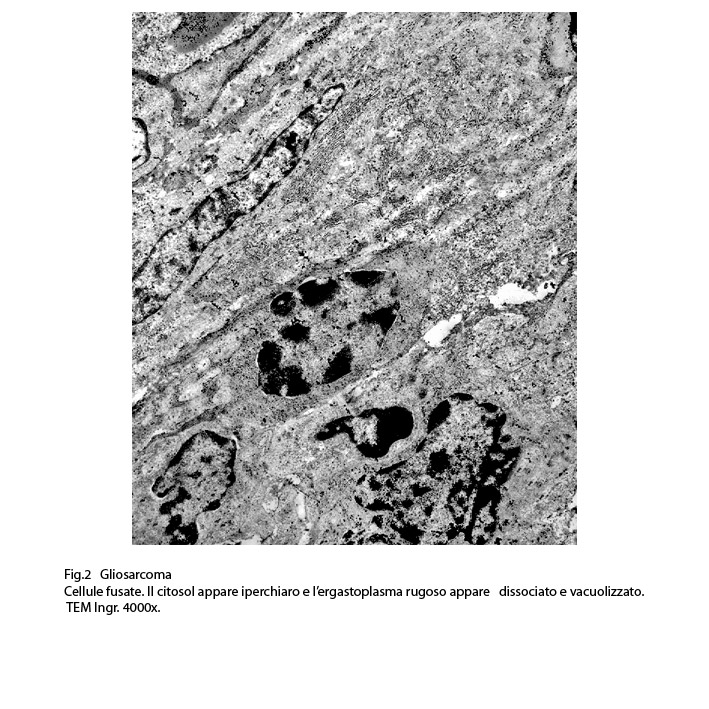 Fig.3
Fig.3 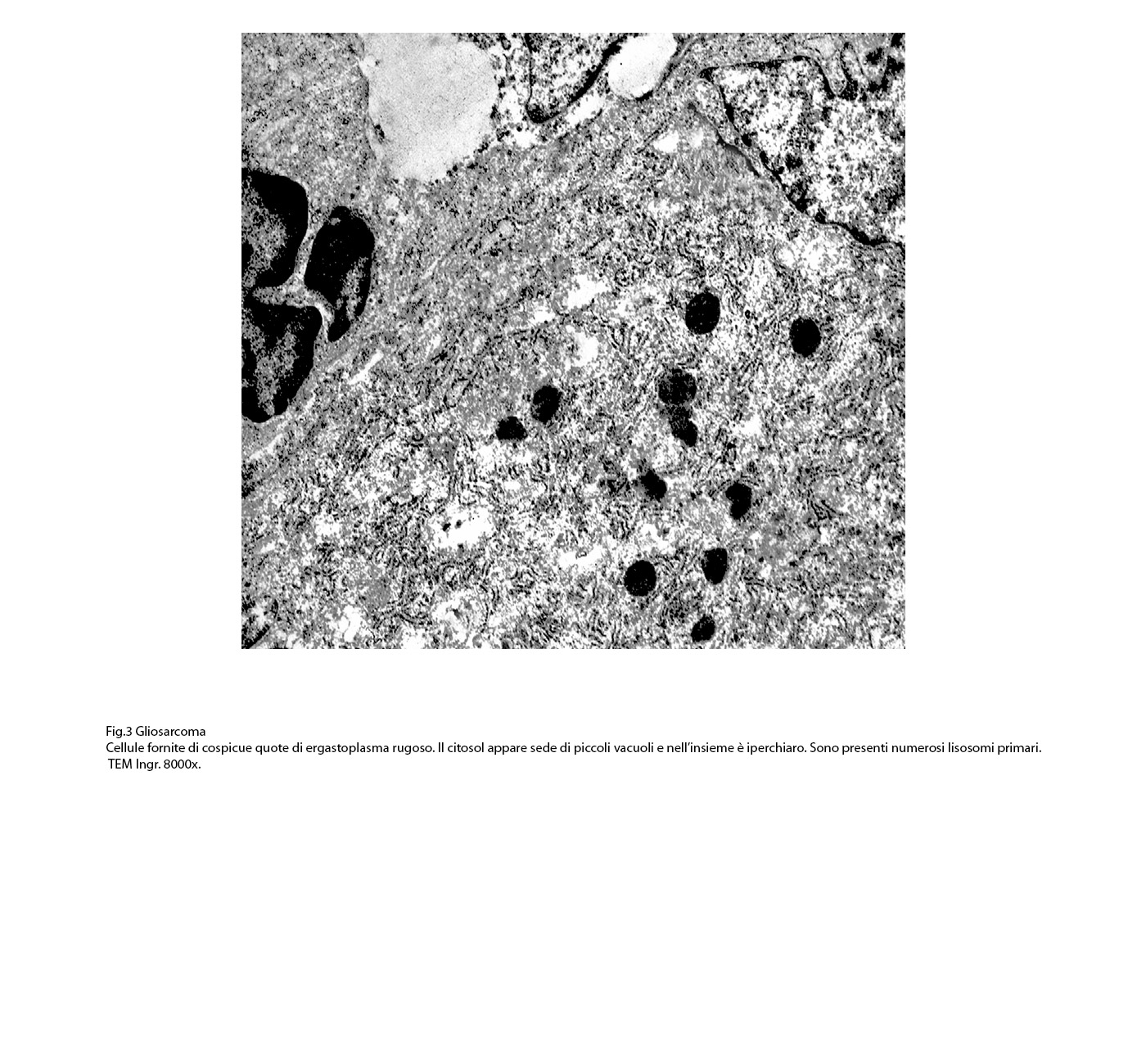
Fig.4 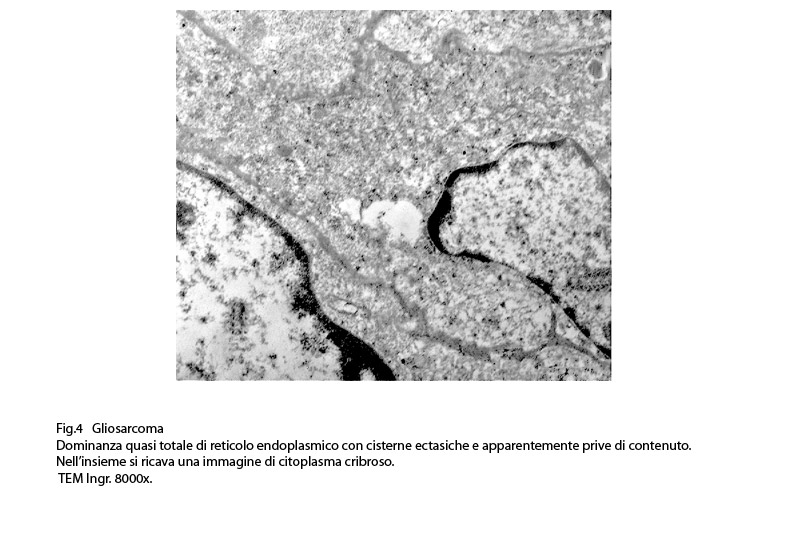
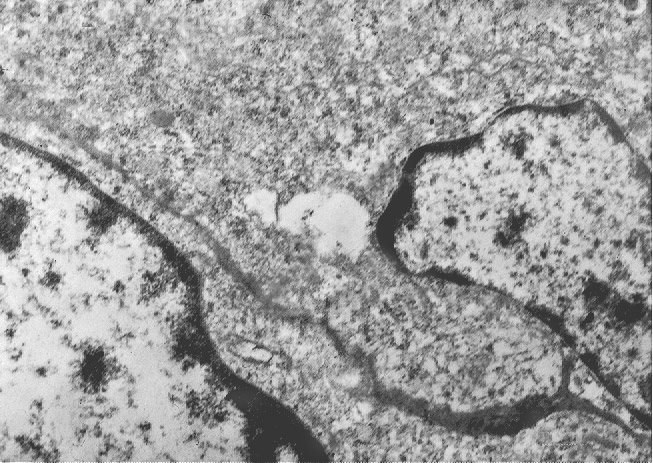
Fig.5 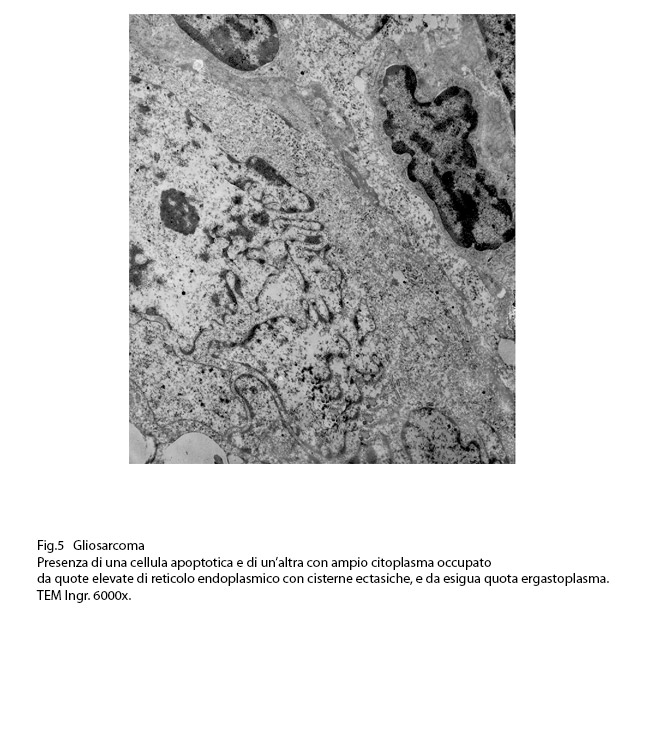 Fig.6
Fig.6 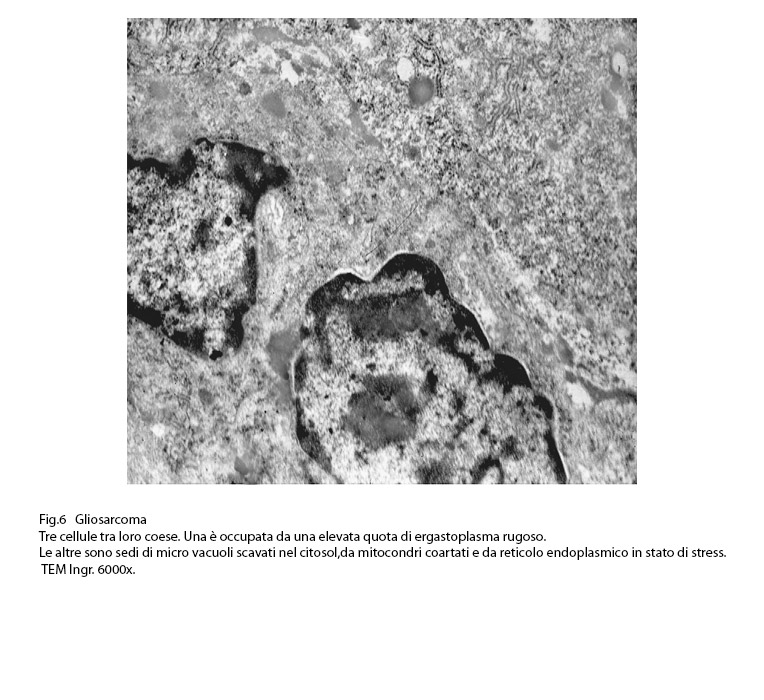
Fig.7 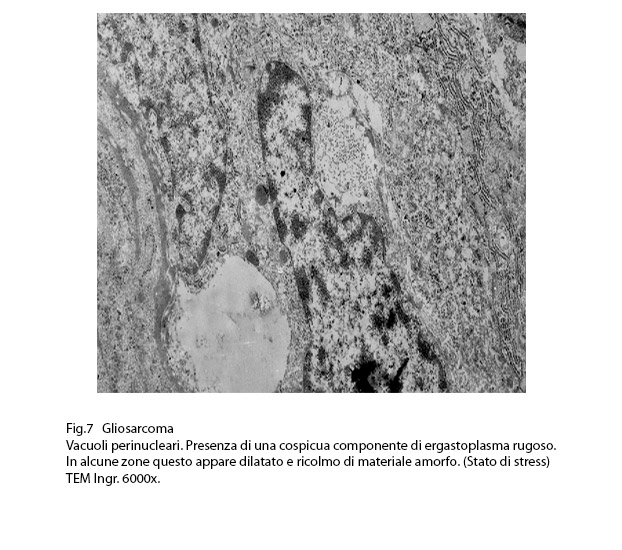
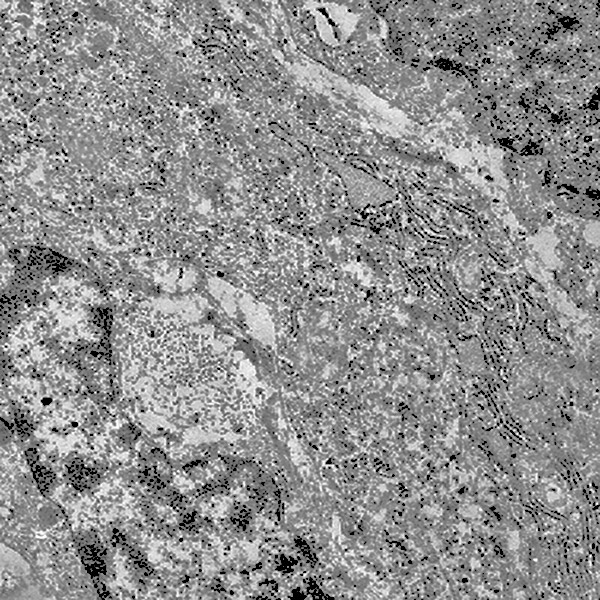
Fig.8 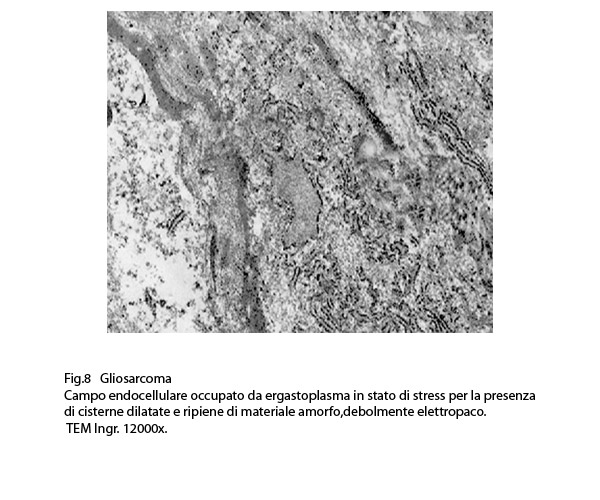 Fig.9
Fig.9 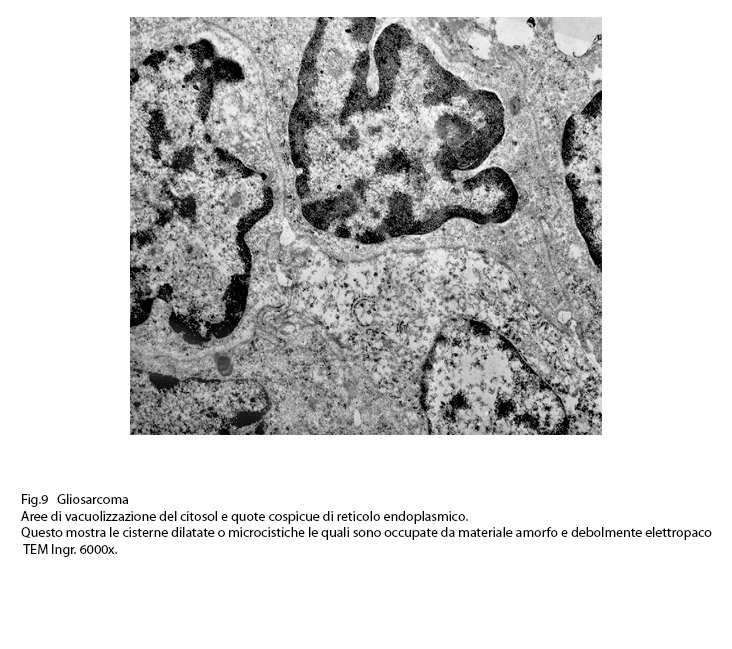 Fig.10
Fig.10 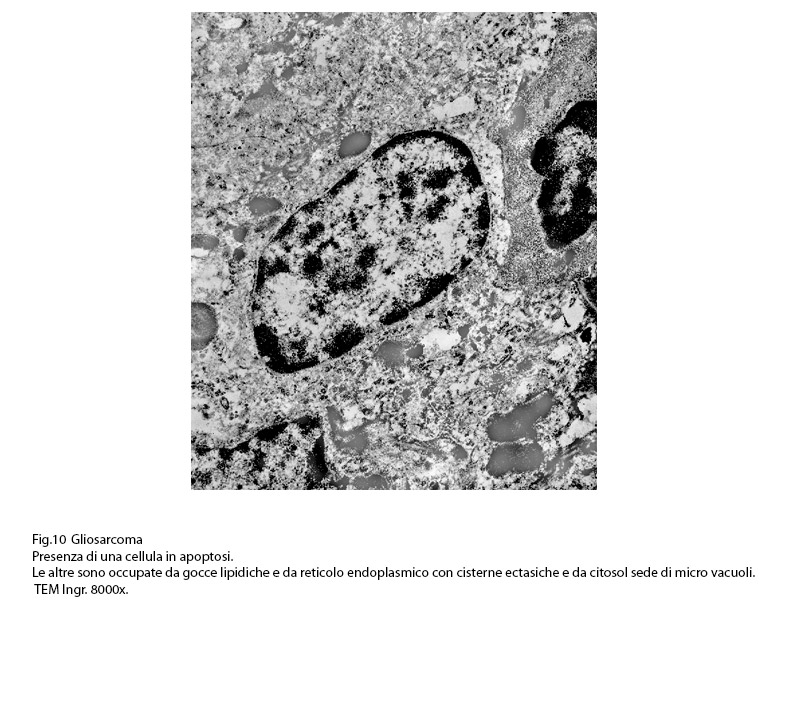
Fig.11  Fig.12
Fig.12 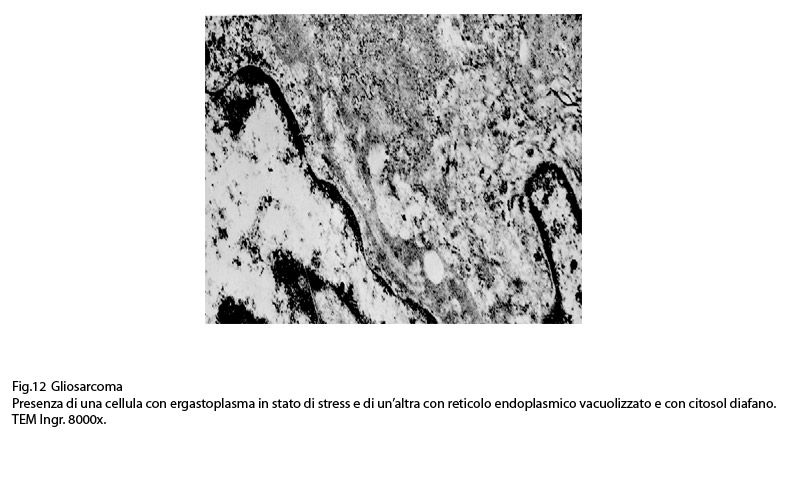
Fig.13 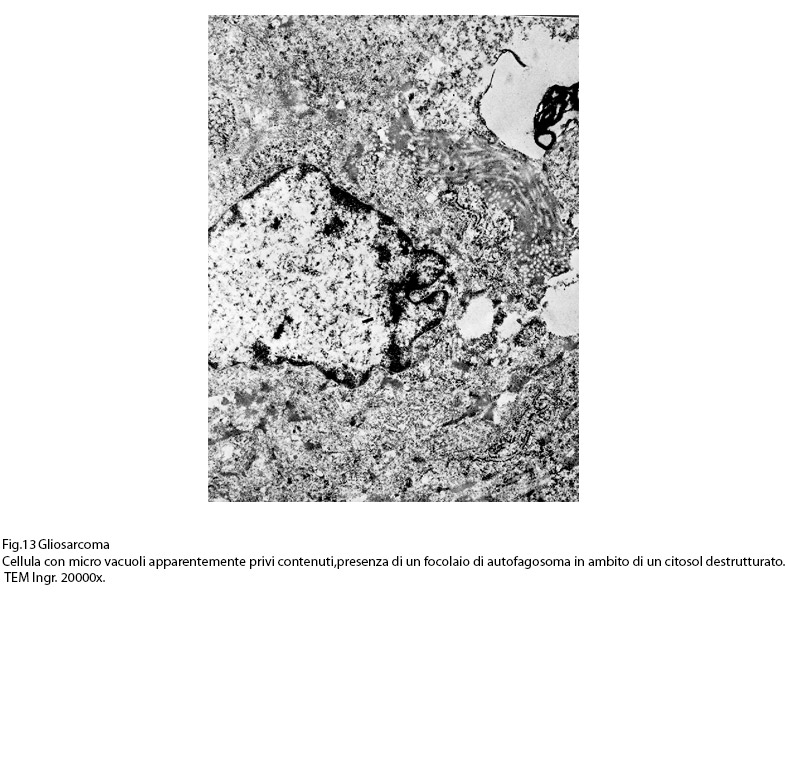 Fig.14
Fig.14 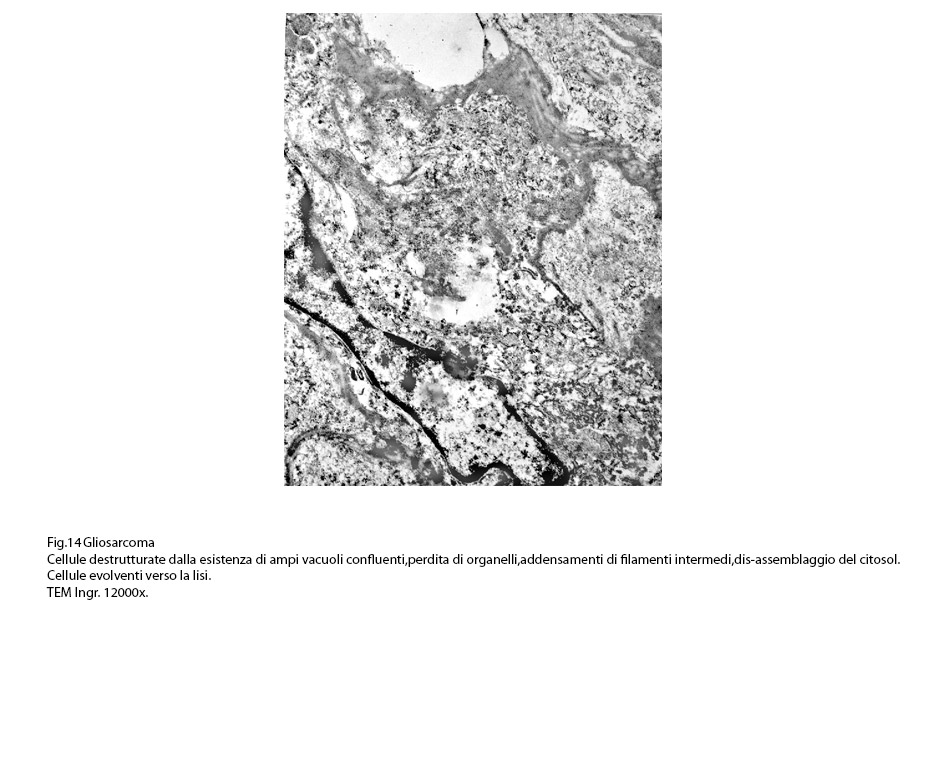
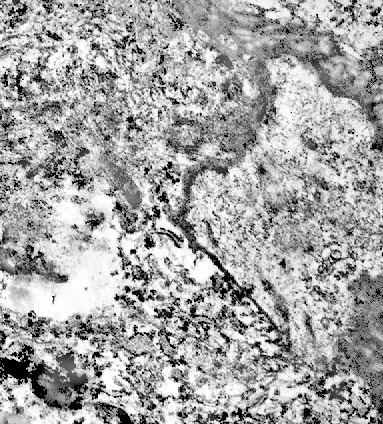
Fig.15 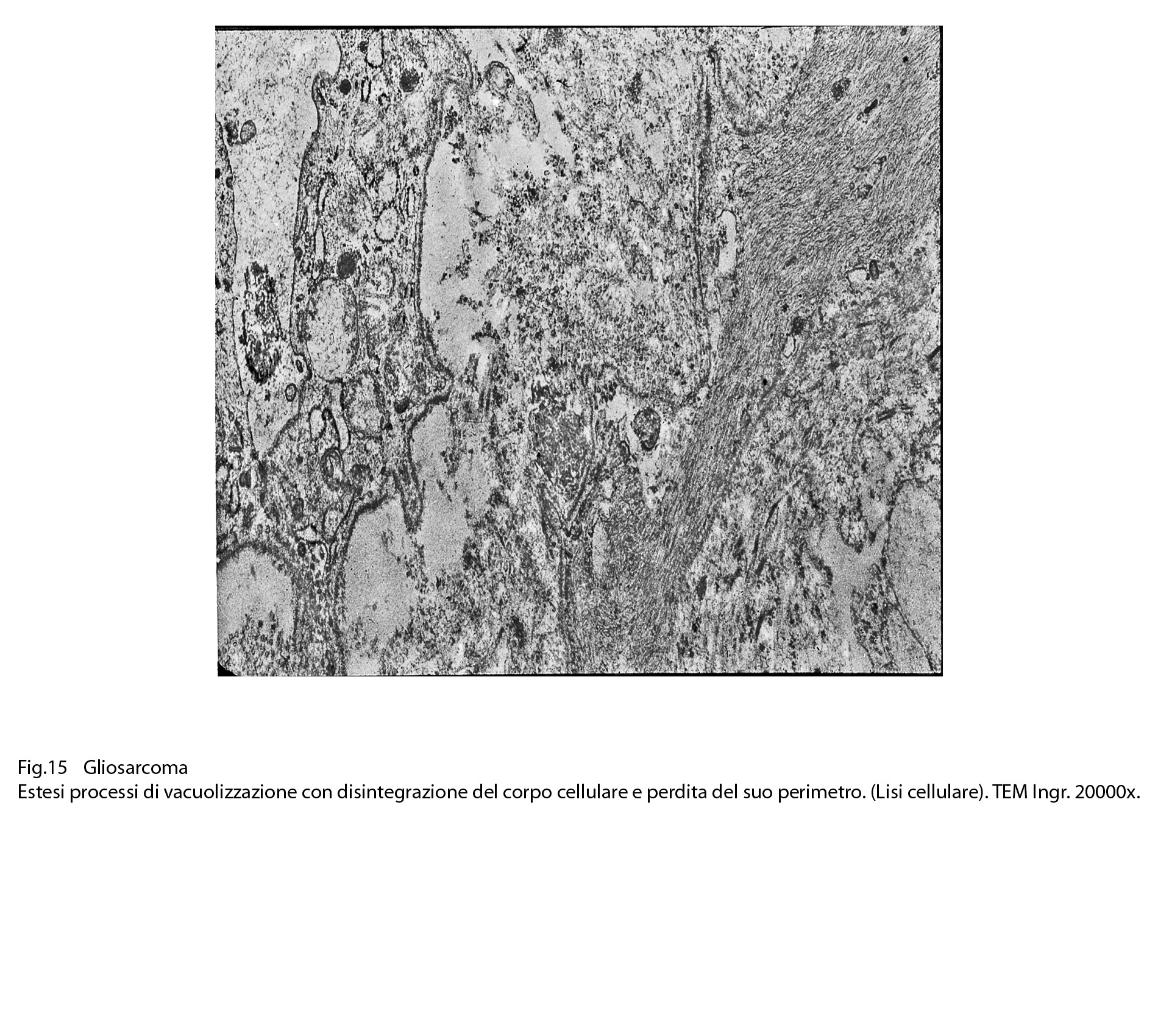
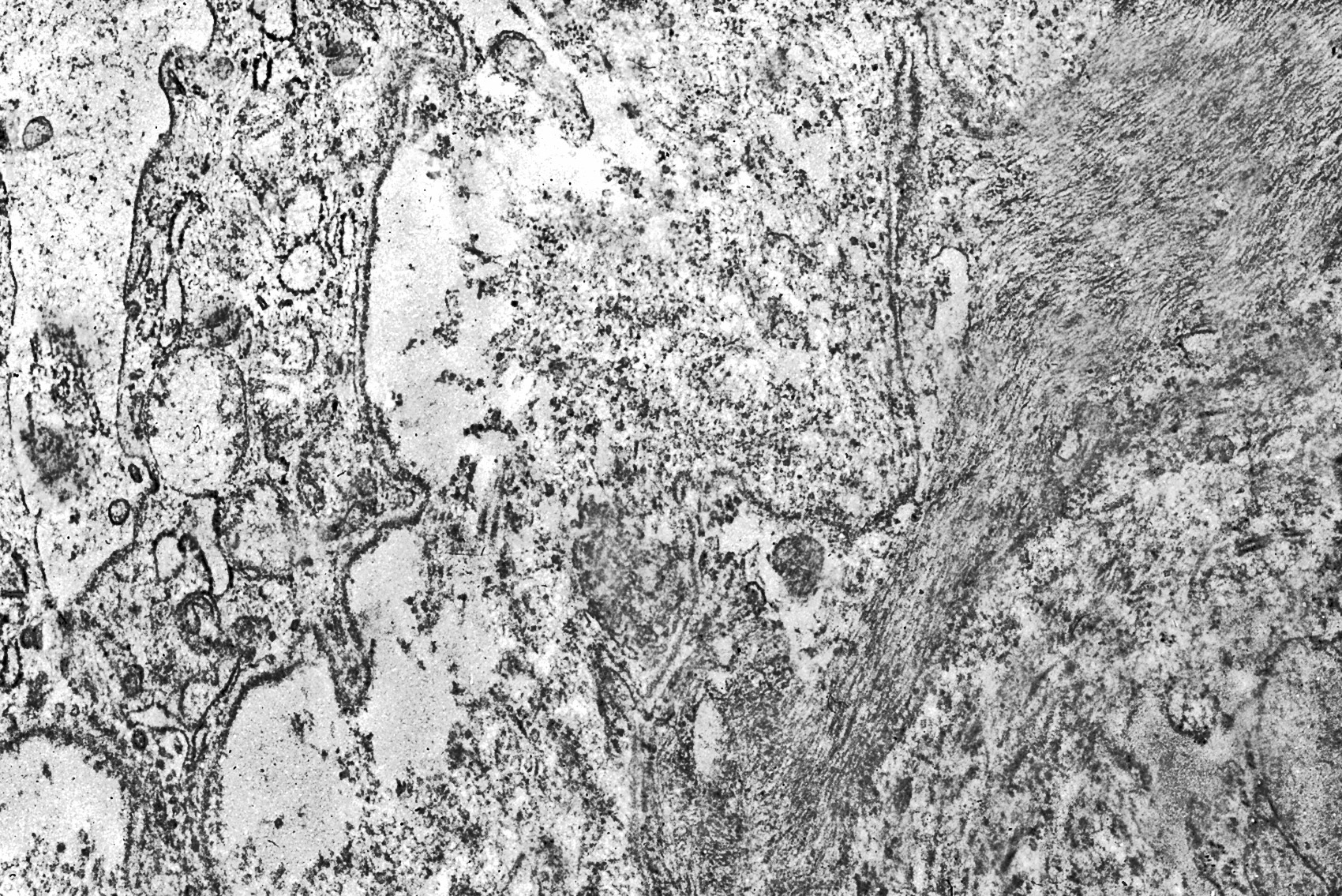
Fig.16  Fig.17
Fig.17 
Fig.18  Fig.19
Fig.19 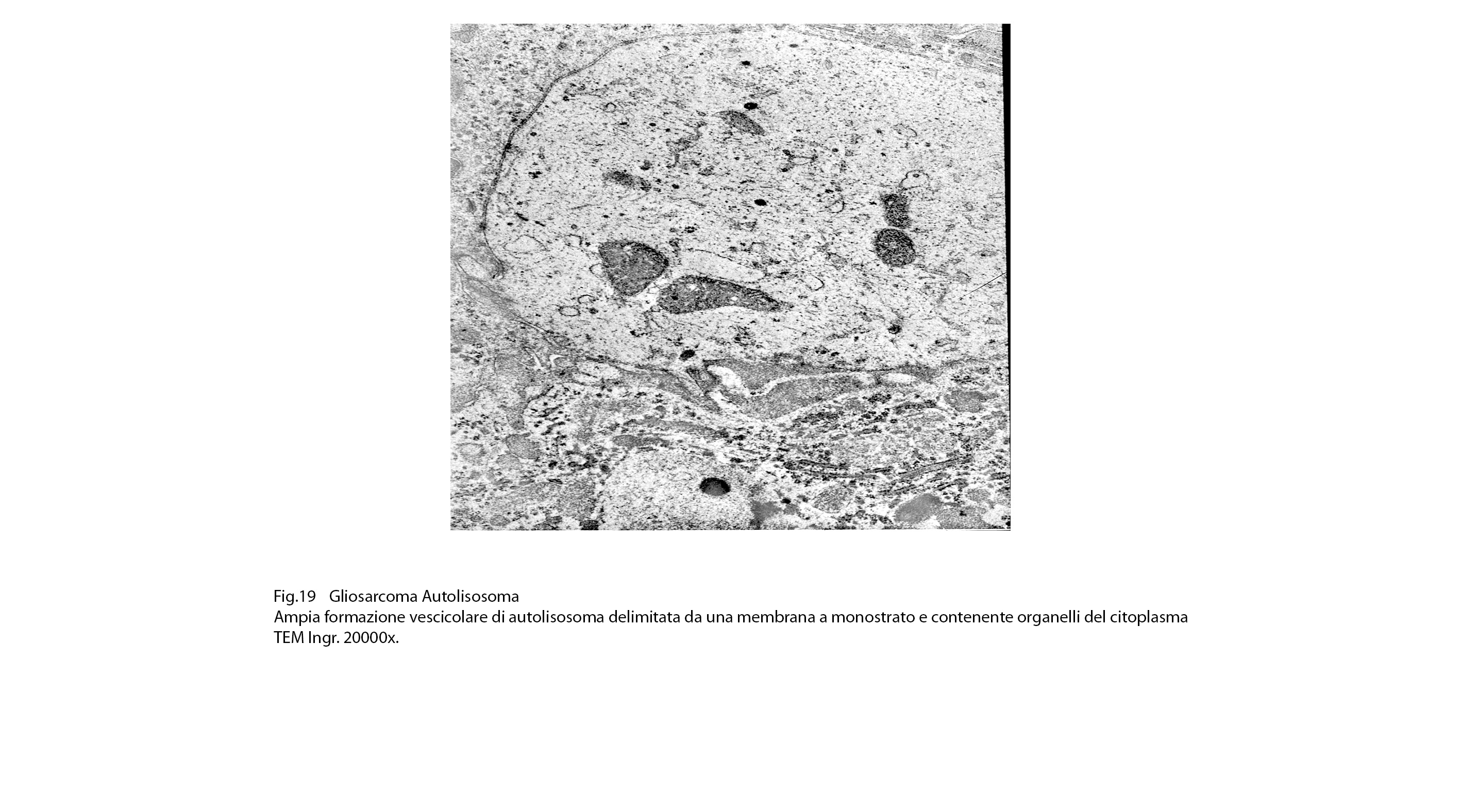
Fig.20 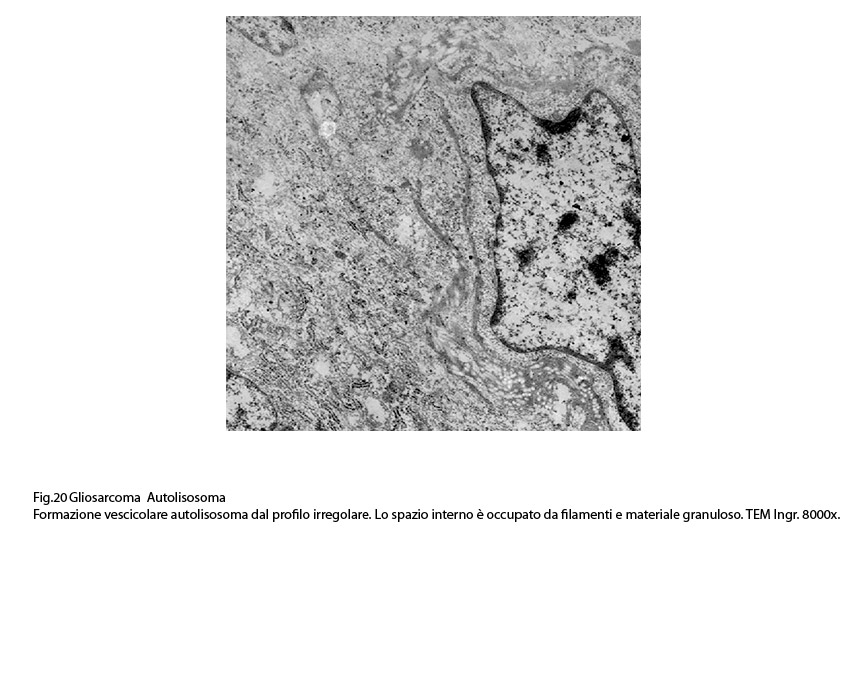 Fig.21
Fig.21 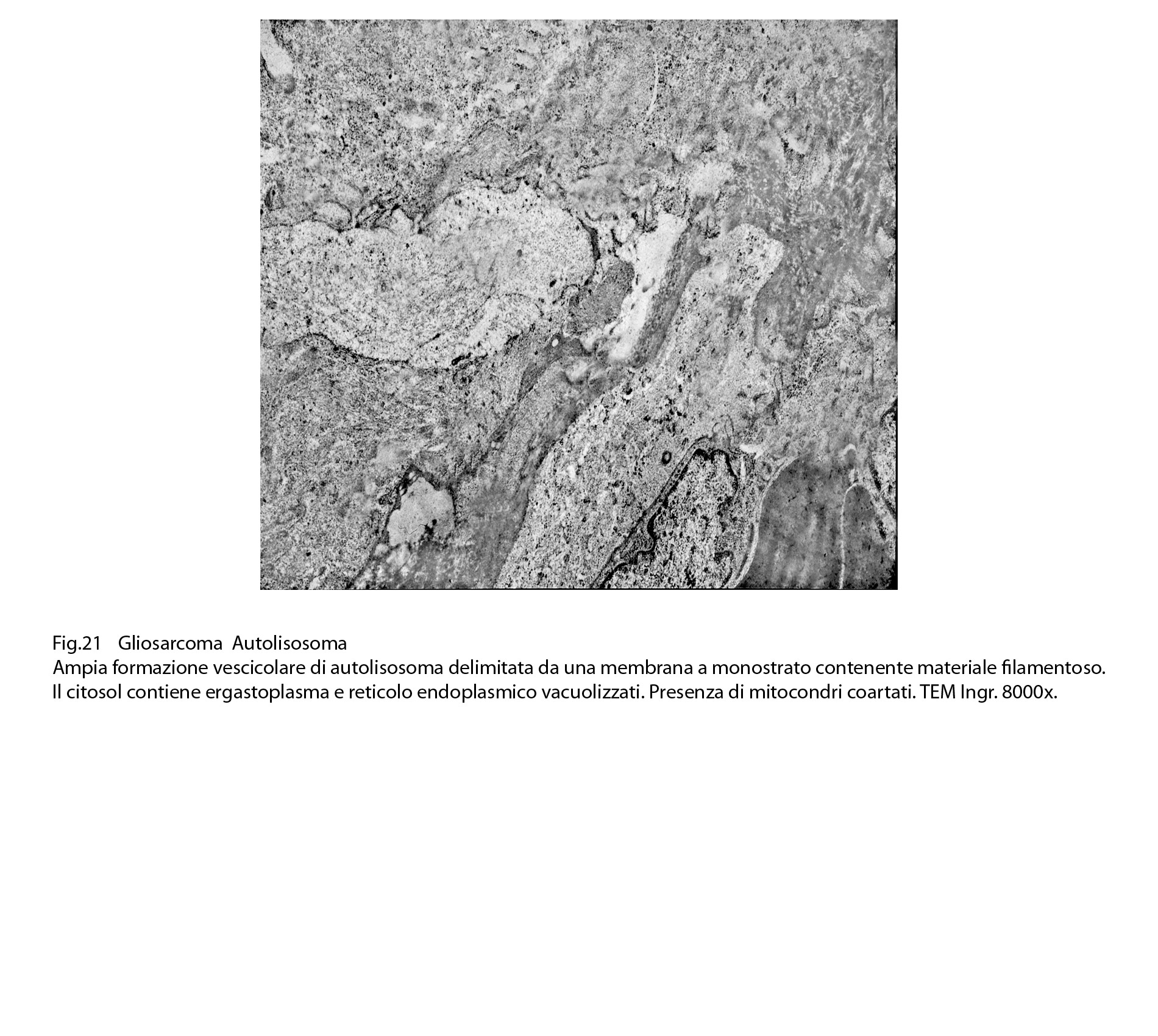
Fig.22 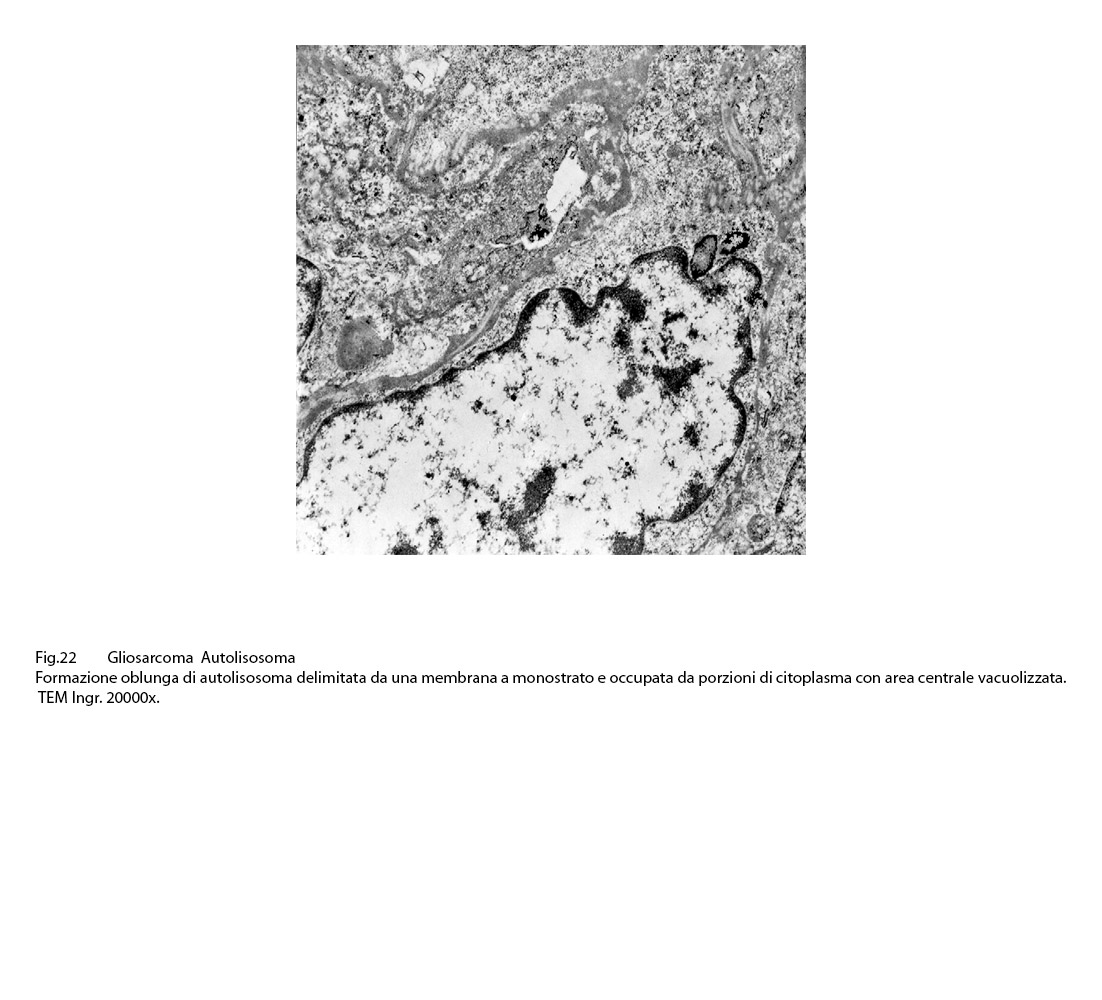 Fig.23
Fig.23  Fig.24
Fig.24 
