ASTROCITOMA ANAPLASTICO
L’astrocitoma anaplastico è una neoplasia di natura astrocitaria, maligna, infiltrante ed è formata da cellule atipiche, scarsamente differenziate.
Esso può manifestarsi come tale dall’inizio (astrocitoma anaplastico primitivo), oppure può essere conseguenza di una trasformazione anaplastica di un astrocitoma diffuso grado II (astrocitoma anaplastico secondario).
Si riconosce al microscopio per uno stato di ipercellularità, per un alto disordine architettonico, per il pleomorfismo anaplastico delle cellule,e non ultimo per il numero delle mitosi tipiche ed atipiche.
Nei casi di astrocitoma anaplastico secondario la trasformazione in senso maligno non si manifesta in modo contemporaneamente globale; essa si appalesa sotto forma di focolaio unico odi focolai plurimi e questi f accrescendosi divengono zonali, sub-totali e infine coinvolgenti l’intera neoplasia preesistente.
Ciascuno di questi focolai è autonomo, è indipendente ed è diacronico rispetto agli altri; pertanto ognuno può essere costituito da elementi anaplastici con livelli diversi di differenziazione e da elementi aventi ancora i caratteri morfologici della variante astrocitaria di origine.
Questo processo di anaplasia può essere secondario a tutte le varianti dell’astrocitoma diffuso di grado II; tra queste la variante gemistocitica evidenzia una maggiore aggressività e consente un periodo più breve di sopravvivenza.
L’astrocitoma anaplastico ha una accentuata tendenza ad acquisire i caratteri isto-morfologici e biologici del glioblastoma multiforme; ciò viene considerato un peggioramento delle condizioni anatomo-cliniche; tale transizione si rivela attraverso un maggior numero di atipie e di mitosi, per il riscontro di “mostruosità nucleari”, per la presenza di cellule giganti plurinucleate e soprattutto per la esistenza di focolai di micro-macronecrosi e la comparsa di numerosi nuovi vasi distribuiti in modo disordinato e strutturati in modo semplificato (neoangiogenesi).
Questo processo di transizione verso il glioblastoma non è globale e rapido; pertanto è molto frequente il riscontro nello stesso reperto esservi lai commistione di strutture anaplastiche e di aspetti glioblastomatosi.
Questo dinamismo dell’astrocitoma anplastico sia per quanto riguarda la sua origine sia per la sua tendenza ad acquisire caratteri glioblastomatosici rende insufficiente la sola istomorfologia; necessitano,pertanto, indagini di immunoistochimica e di genetica-molecolare.
L’astrocitoma anplastico colpisce soprattutto soggetti adulti e interessa tutte le sedi ove affiorano l’astrocitoma diffuso; tuttavia, i dati statistici segnalano una maggiore incidenza di questa neoplasia a livello degli emisferi cerebrali.
Caratteri macroscopici
Abitualmente l’astrocitoma anaplastico, allo esame macroscopico appare al tatto di consistenza molle , friabile, granuloso; il colore di base è grigio-giallastro con possibili punteggiature rosso-emorragiche. I limiti sono sfumati o indistinti in conseguenza della entità dei processi di infiltrazione delle cellule neoplastiche nei tessuti sani circostanti.
In casi di astrocitoma anplastico secondario a sviluppo plurifocale e/o plurizonale si riscontrano aspetti disomogenei per consistenza e colore; infatti si ritrovano zone di consistenza sostenuta accanto ad altre di consistenza molle-friabile e il colore grigio di base viene in parte mascherato dalle zone di colore rosso per emorragie e dalle zone gialle per processi regressivi.
Nei casi in cui il tumore acquisisce il profilo del glioblastoma alcuni di questi caratteri si accentuano ed altri subentrano e tra questi i focolai di necrosi.
Caratteri microscopici
A Caratteri istopatologici
L’esame istopatologico mette in evidenza un astrocitoma avente i caratteri citomorfologici di una neoplasia maligna: si ritrova,infatti, uno stato di ipercellularità senza coesione intercellulare e senza una disposizione spaziale strutturata,inoltre si rileva una condizione di pleomorfismo cellulare associato a marcata atipia nucleare e a numerose mitosi.
Fig.1 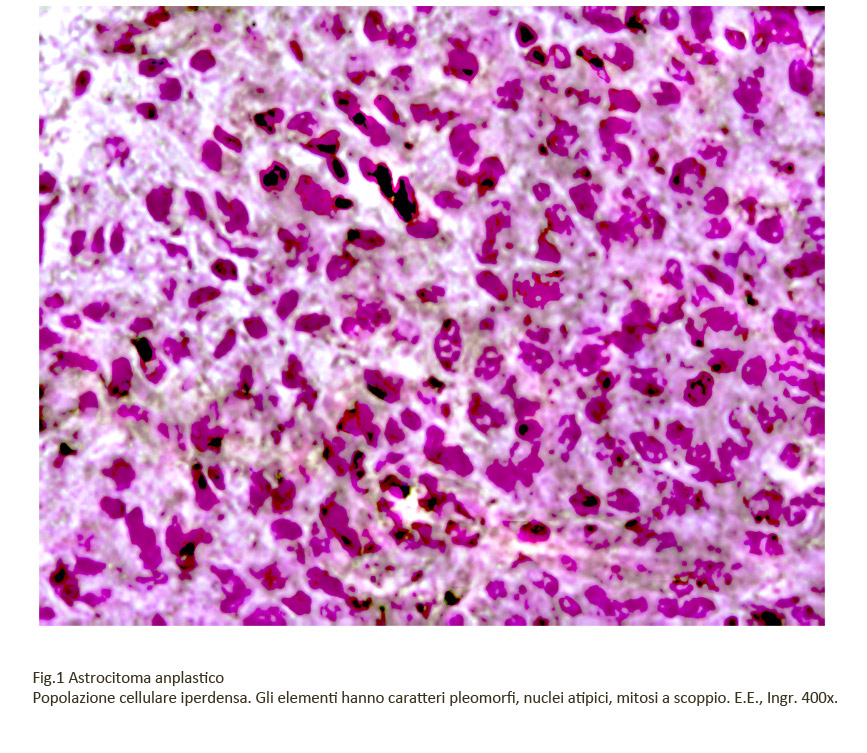 Fig.2
Fig.2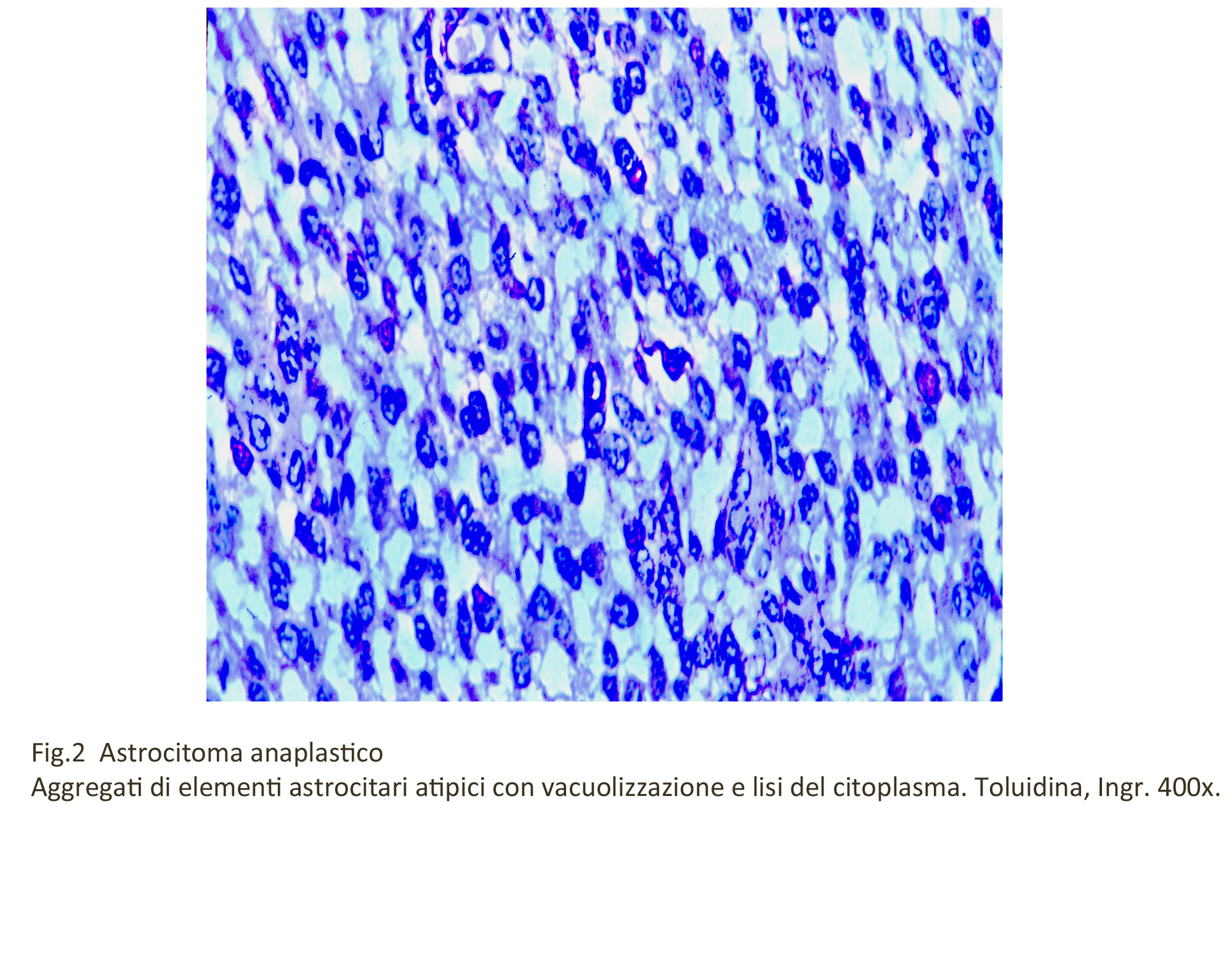 Fig.3
Fig.3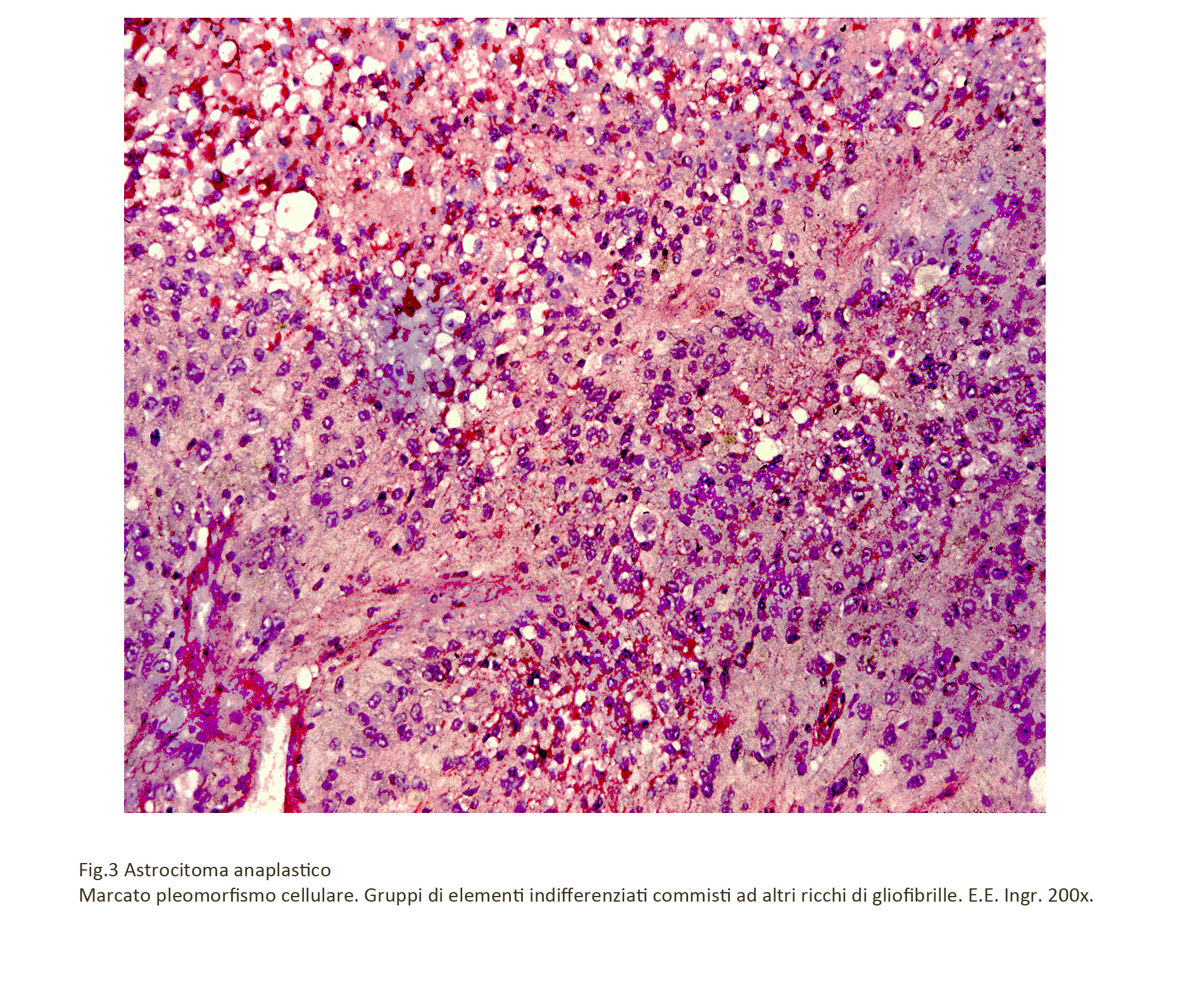
Nel contesto di una popolazione iperdensa e monomorfa si possono repertare elementi binucleati e
Plurinucleati.
Fig.4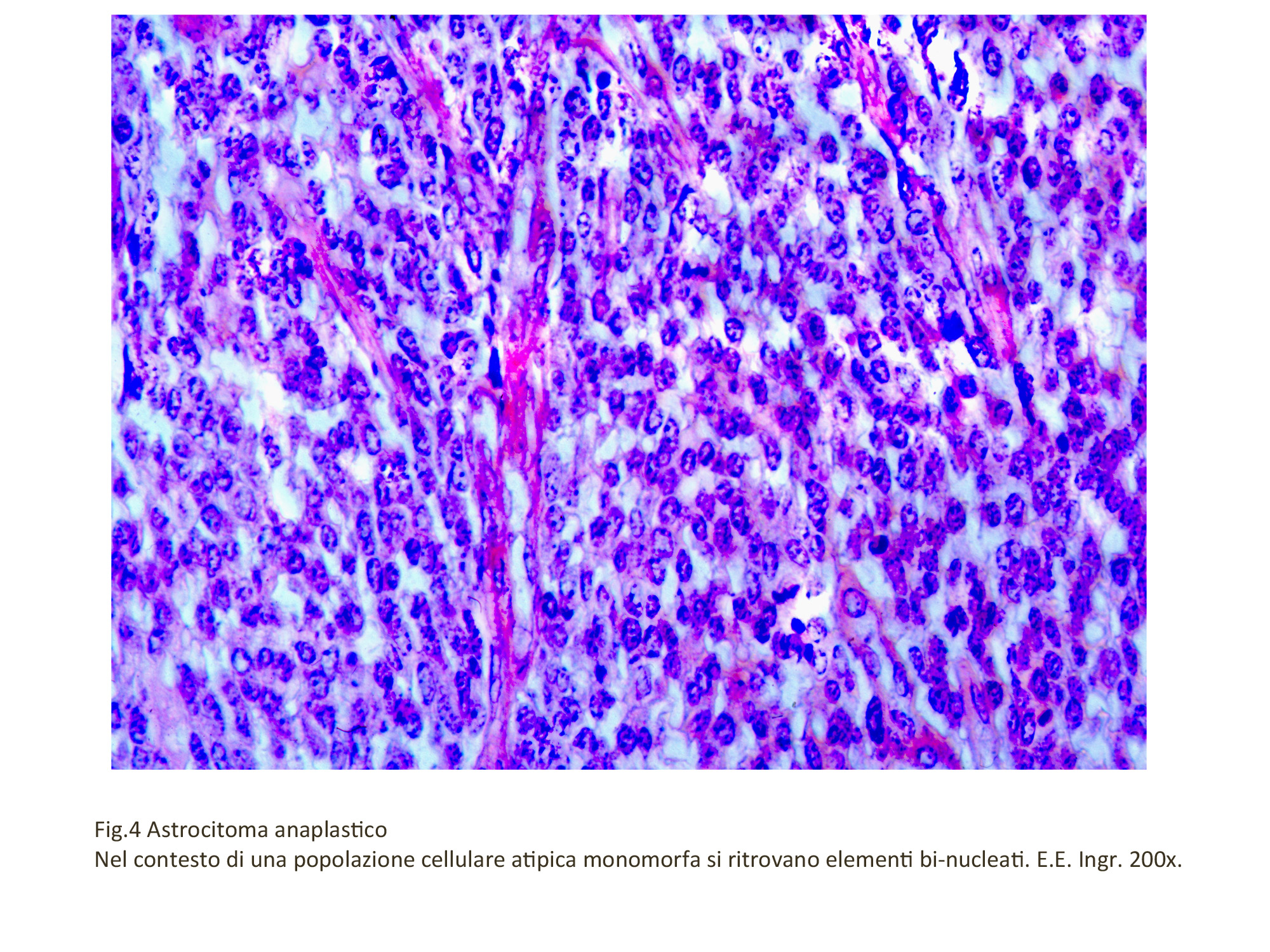 Fig.5
Fig.5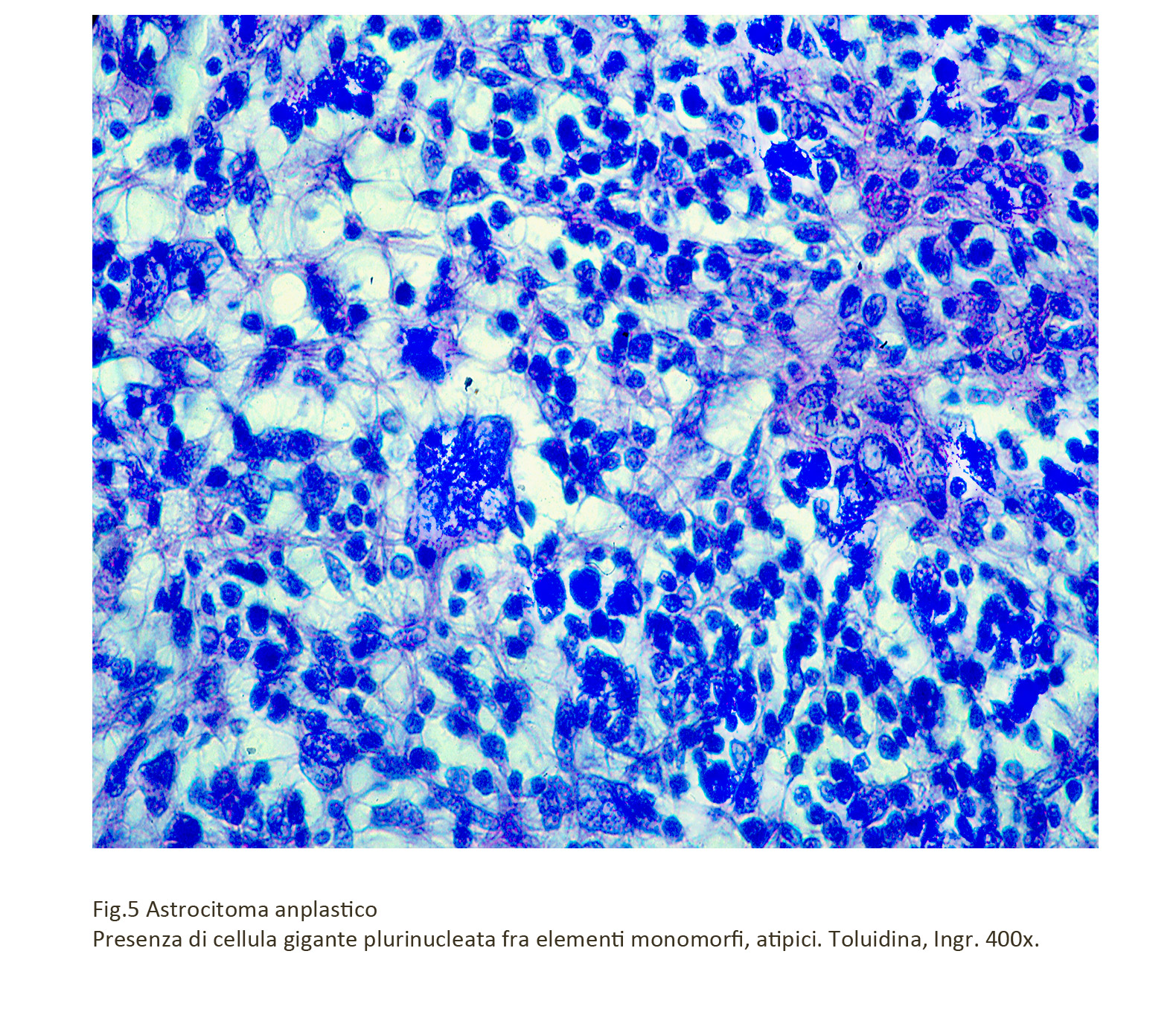
Nei casi di astrocitoma anplastico secondario la trasformazione neoplastica in senso maligno ha origine da tutte le varianti dell’astrocitoma diffuso; questa trasformazione avviene in modo transizionale per gradi e ciò appare evidente nei casi di astrocitoma anaplastico plurifocale e plurizonale; infatti, è possibile repertare nello stesso campo microscopico commiste a cellule anplastiche altre aventi i caratteri dell’astrocitoma diffuso di partenza. Alla stessa maniera si ritrovano elementi aventi una citomorfologia intermedia, secondo la quale si ritrovano i caratteri nucleari della malignità con quelli citoplasmatici ancora in parte conservato.
Come è stato già ricordato,gli astrocitomi anplastici secondari ad astrocitoma gemistocitico hanno una maggiore aggressività biologica e un periodo di sopravvivenza più breve;ciò è motivo di ulteriori interrogativi risolvibili solo mediante esami microscopici analitici e dettagliati per escludere la presena di quote gemistocitiche in tutti i casi di astrocitoma anaplastico. (Journal of Neurosurgery, 2013, 119, 434-41).
Fig.6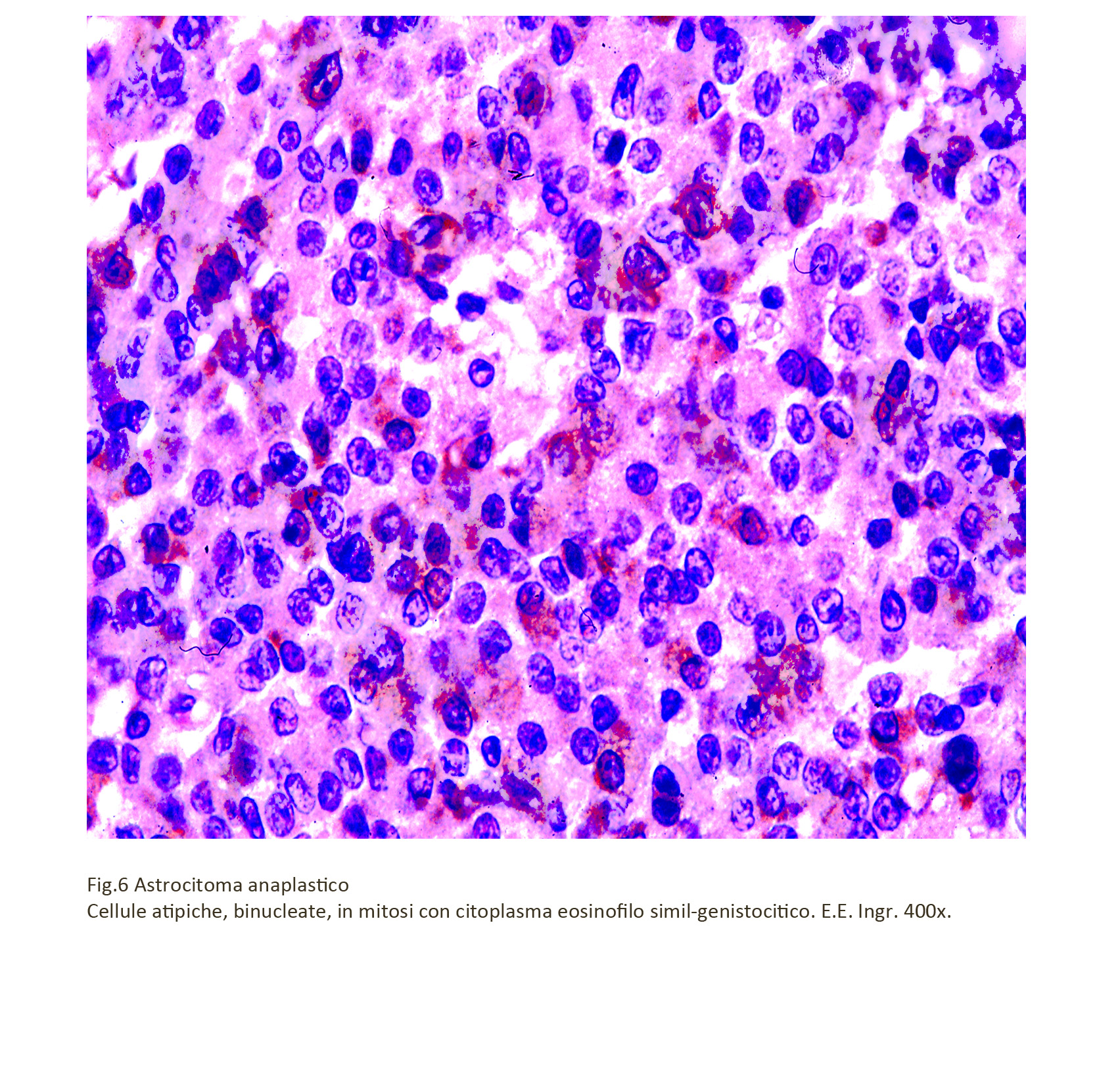
Molto frequentemente cellule anaplastiche avvolgono e infiltrano le pareti dei vasi,inducendo cosi una diffusione neoplastica per via sistemica.
Fig.7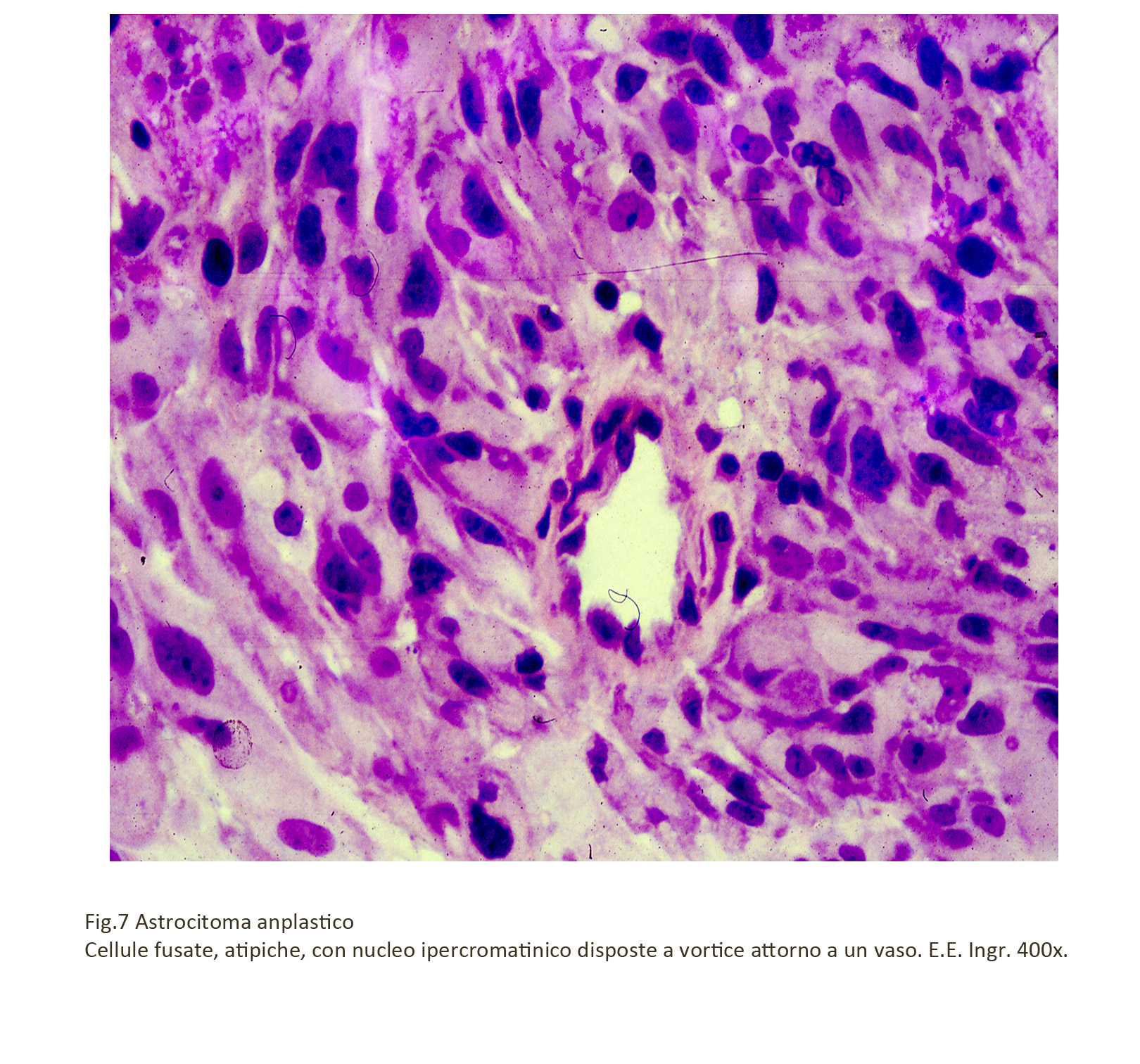 Fig.8
Fig.8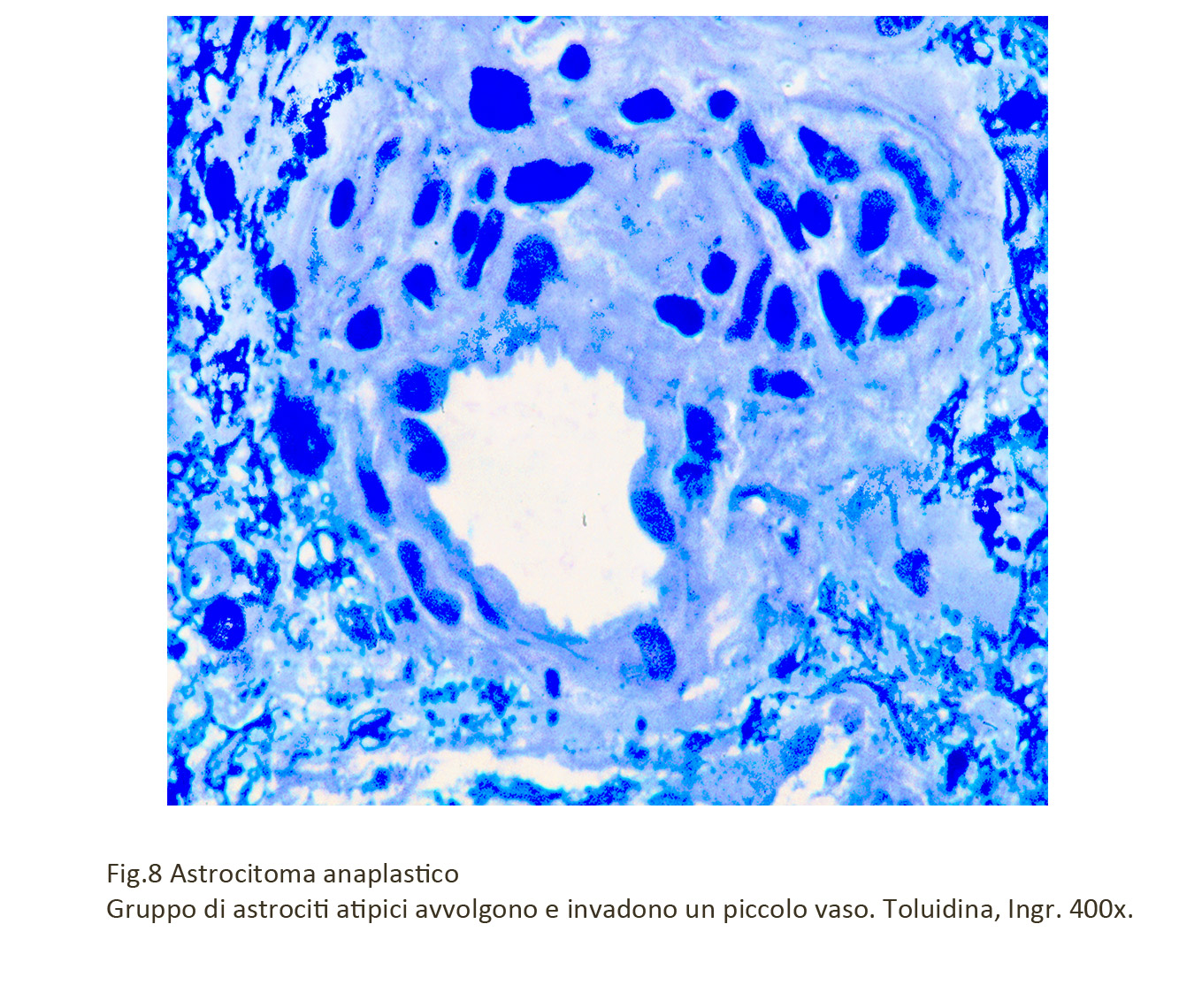
E’ possibile repertare nel contesto di un caso di astrocitoma anaplastico are di necrosi e di neoangiogenesi,significative della presenza di foci di trasformazione avanzato verso un glioblastoma multiforme.
Fig.9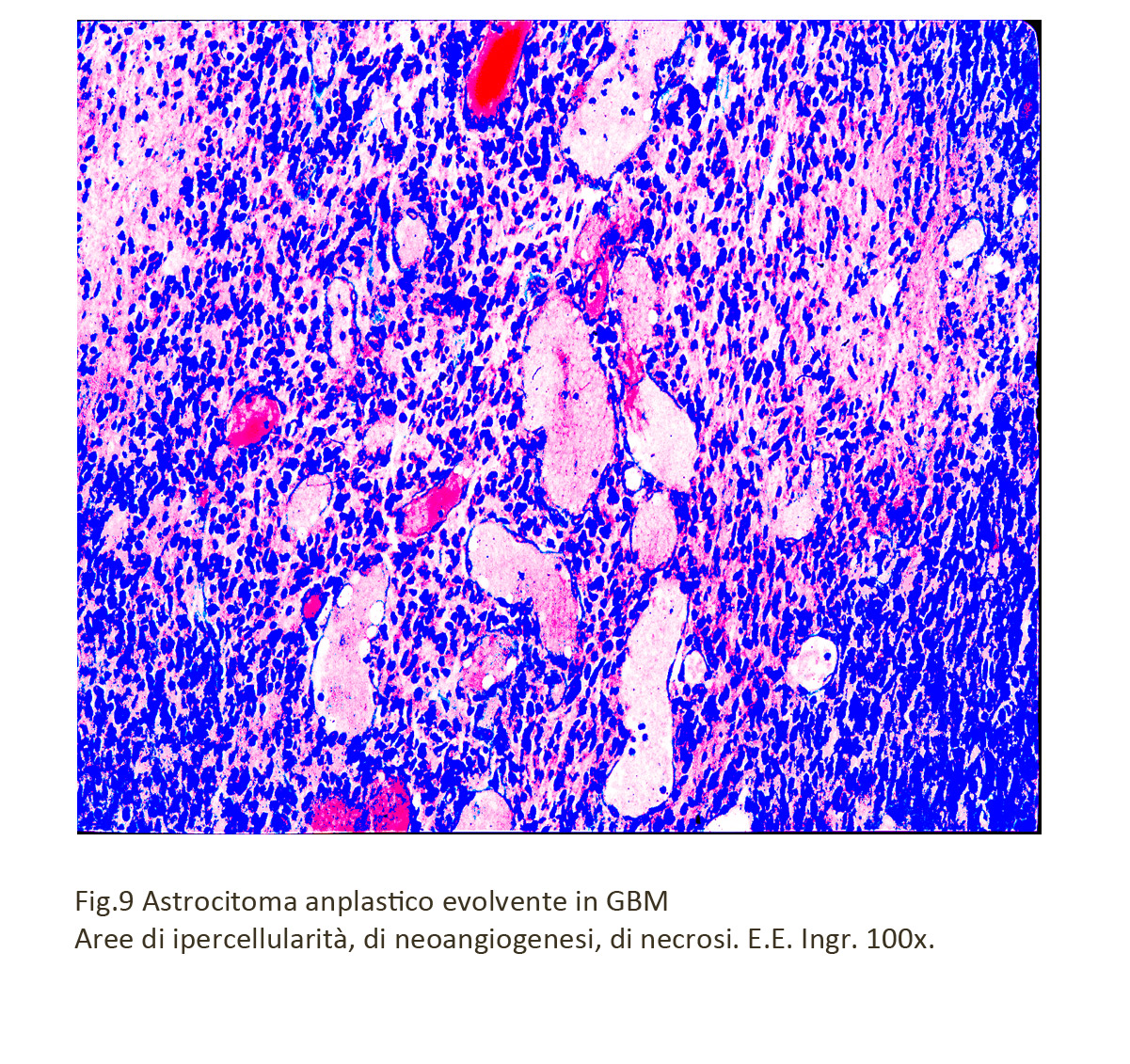
Questo esame istopatologico seriato consente anche di controllare nei dettagli la eventuale esistenza di focolai di necrosi e/o di processi di neoangiogenesi per escludere il passaggio verso il glioblastoma multiforme.
- Indagini di immunoistochimica
-
Le osservazioni di istopatologia devono essere integrate da ricerche di immunoistochimica finalizzate alla identificazione della natura delle cellule neoplastiche e del loro indice di attività proliferativa.
La natura astrocitaria della neoplasia viene confermata mediante la immunoespressività delle cellule per la proteina GFAP e la Vimentina.
Fig.10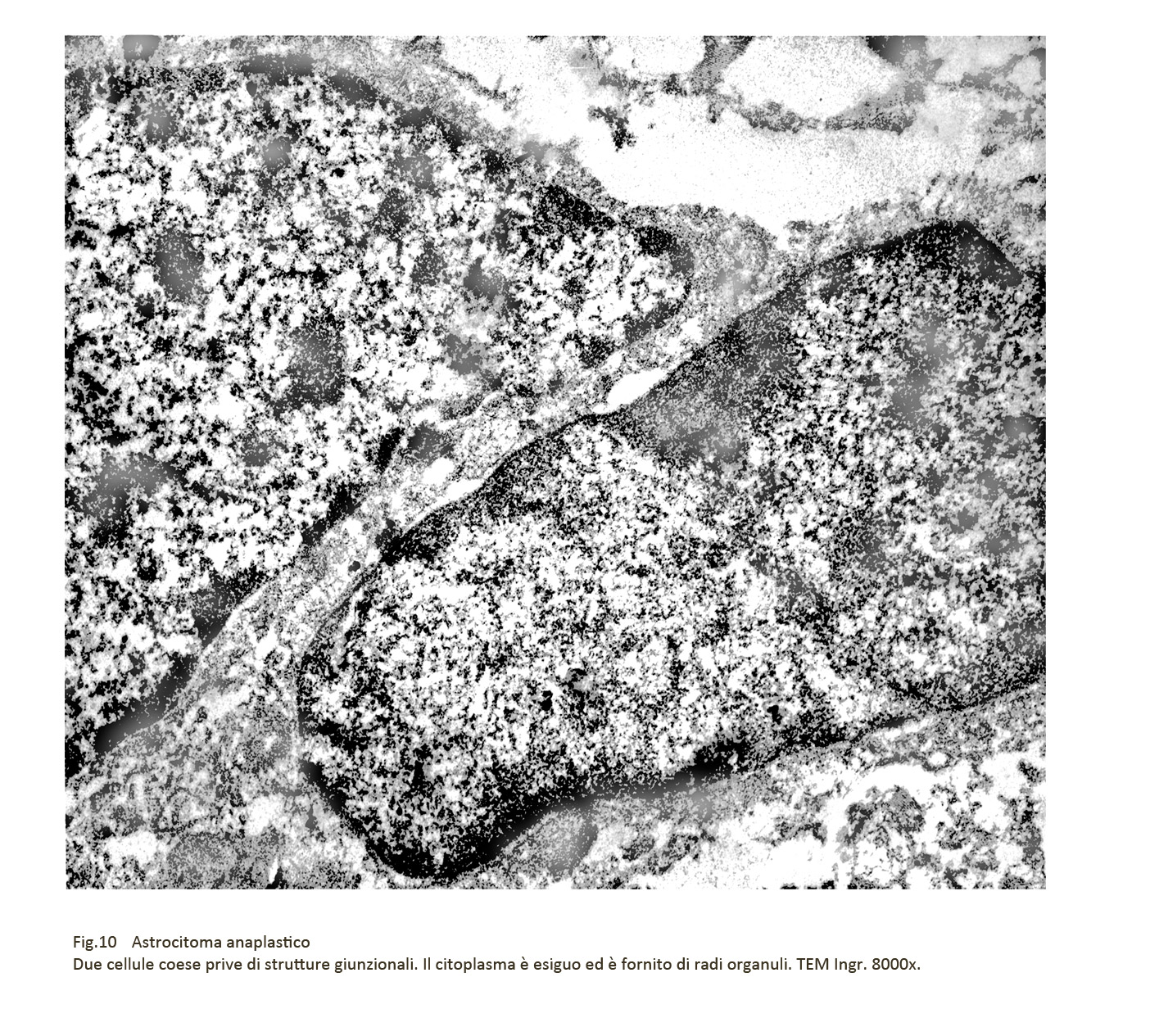 Fig.11
Fig.11
Fig.12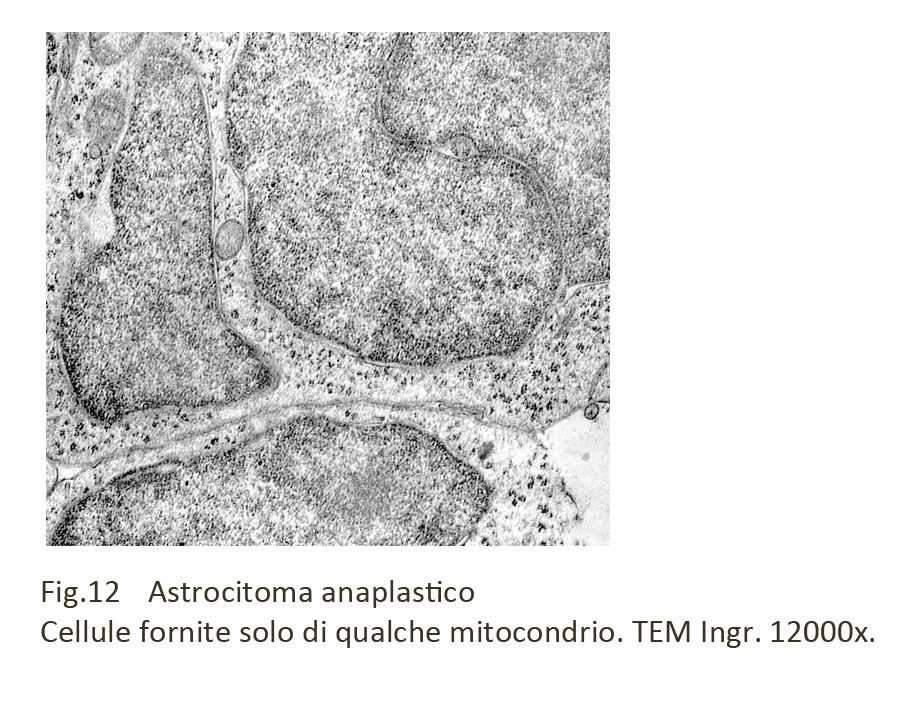 Fig.13
Fig.13
L’indice di proliferazione è documentato tramite la espressività immunologica del Ki67/Mib-1.
(J. Cancer Res. Ther. 2014, 10, 641-5)
(Int. J. Clin. Pathol., 2014, 7, 8905-10)
(J. Cancer Research Therapeuties, 2014, 10, 641-5).
- Caratteri ultrastrutturali
Il livello di marcata anaplasia può essere evidenziato anche mediante osservazioni al microscopio elettronico. Il citoplasma delle cellule di questa neoplasia si mostra esiguo, povero di organuli e a struttura compatta. Solo in alcune cellule è possibile osservare nella matrice citoplasmatica sottili fasci di gliofibrille.
Fig.14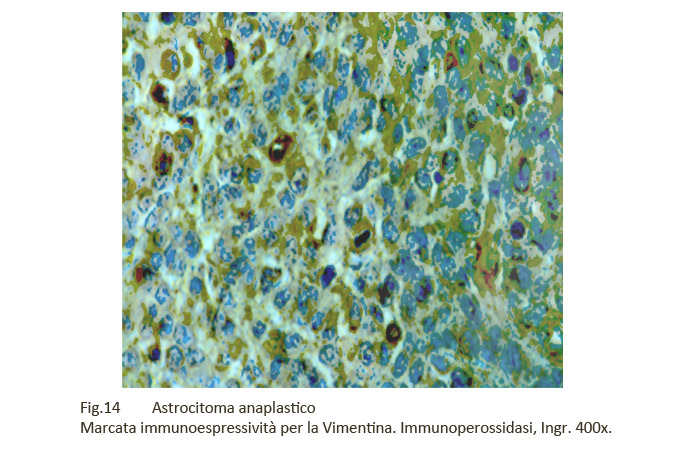 Fig.15
Fig.15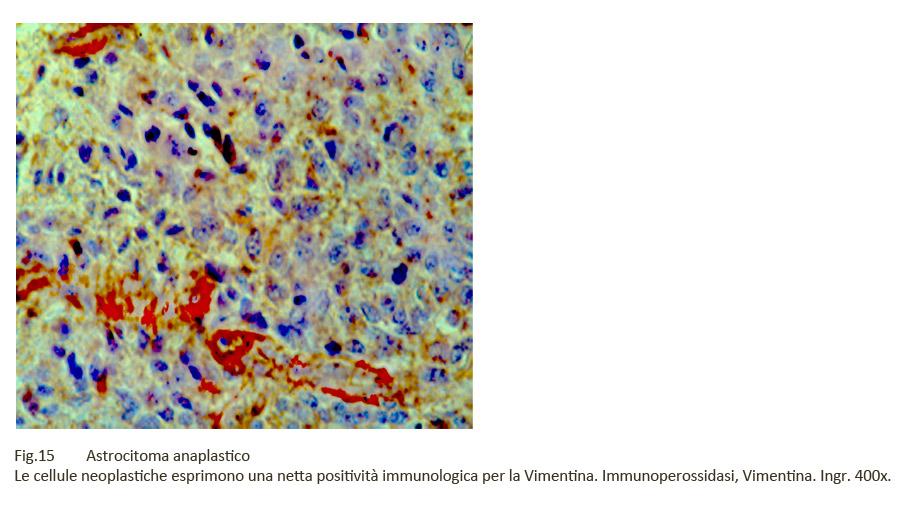 Fig.16
Fig.16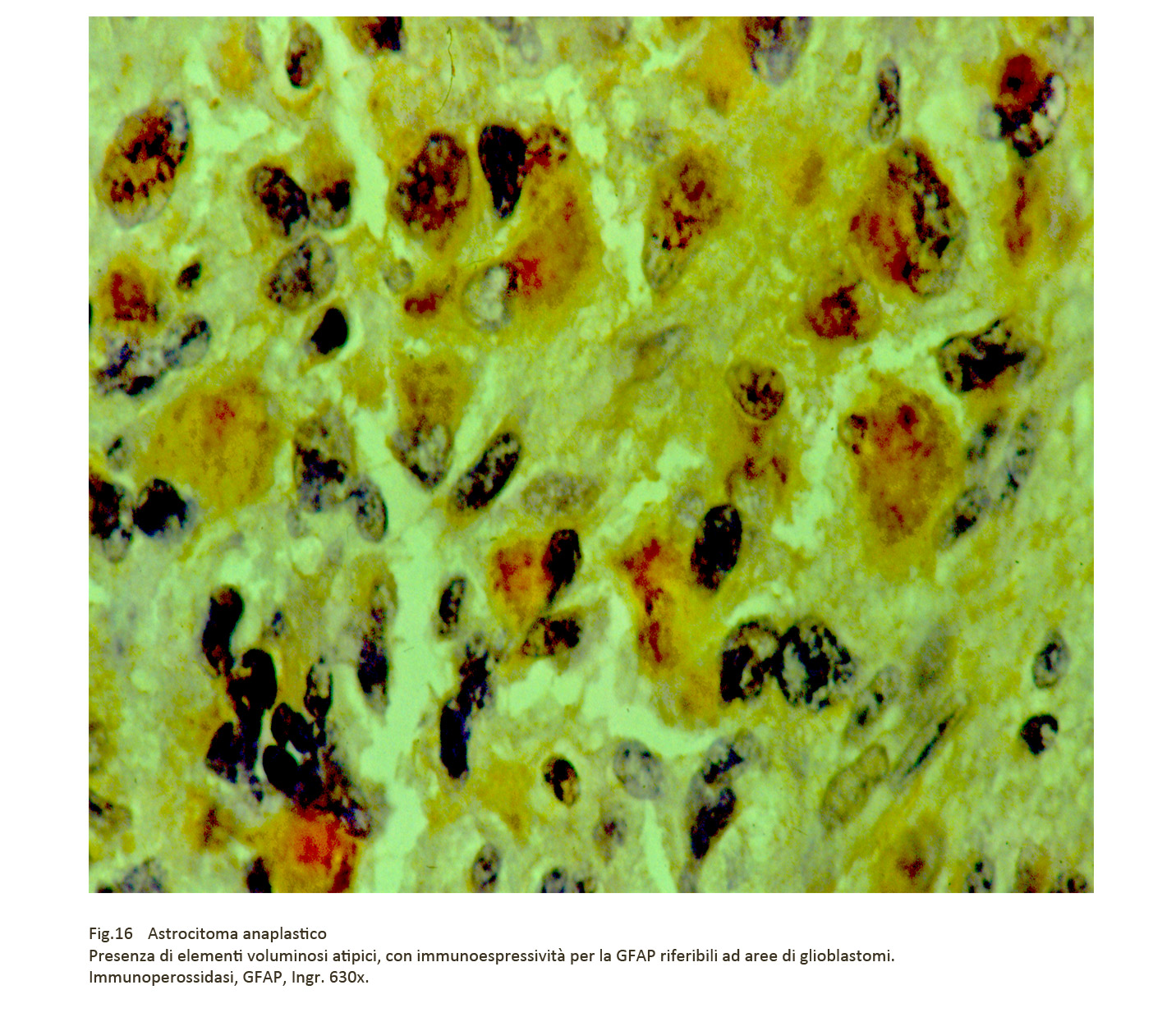
- Caratteri genetico-molecolari
Come è noto, nei processi di anaplasia si evidenzia una dis-regolazione del ciclo cellulare; questo stato di cose può essere documentato mediante indagini genetico-molecolari.
Esse forniscono informazioni circa la natura della neoplasia, la sua aggressività biologica, i controlli circa l’efficacia dei trattamenti terapeutici e infine la curva temporale di sopravvivenza.
Anche lo studio riguardante gli astrocitomi anaplastici si avvale di queste nuove possibilità, acquisendo così ulteriori certezze diagnostico-prognostiche.
L’assetto genetico-molecolare utilizzato per la diagnostica degli astrocitomi anaplastici è molto articolato e in sintesi si compone delle mutazioni e delle espressività delle seguenti molecole:
- Mutazione di JDH1 e TP53 con perdita delle espressività di ATRX e CDKN2A
(J. Neuropathol. Exp. Neurol. 2015, 74, 442-52) /J. Neurooncol. 2015, 121, 479-81)
- Iperespressività del PC4, coattivatore trascrizionale nei processi di replicazione del DNA
(J. Neurol. Sci. 2014, 15, 293-8)
- Espressività del gene AEG-1 in rapporto al grado degli astrocitomi; essa è alta negli astrocitomi anplastici e nei glioblastomi.
(Int. J. Clin. Exp. Pathol., 2014, 7, 5038-44)
- Sono stati rilevati nei glioni maligni mutamenti di PTEN, EGFR, P16 e perdita della etrozigosità del cromosoma 10
(World J. Surg. Oncol. 2014, 12, 185-90)
- E’ riportato in letteratura che la fusione dei geni KIAA1549: BRAF non è specifica degli astrocitomi pilocitici ma si reperta anche in casi di astrocitoma anaplastico, di glioblastoma, di xanto-astrocitoma pleomorfo anaplastico
(Pediatr. Blood Cancer, 2015, 62, 724-7)
- E’ stato rilevato un rapporto tra livelli di micro-RNA e grado di anaplasia e di attività proliferativa degli astrocitomi.
(Am. J. Cancer Res. 2015, 5, 201-218)
7 Espressività negativa di JDH1/MGMT e iperespressività di p53 indicano una prognosi sfavorevole e un tempo di sopravvivenza ridotto.
(Neuropathol. 2015, 35, 324-35)

